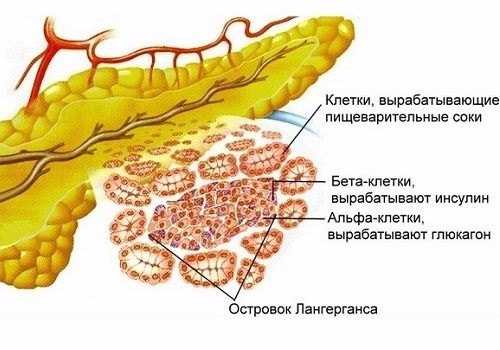
Функции и патология островков Лангерганса: сбой выделяемых гормонов
В самой железе островков немного: они составляют 1—2% от всей массы органа. Клетки островков Лангерганса разнятся между собой по строению и функциям. Имеется 5 их видов. Они секретируют активные вещества, регулирующие углеводный обмен, пищеварение, могут участвовать в ответе на стрессовые реакции.
Что такое островки Лангерганса?
Островки Лангерганса (ОЛ) — это полигормональные микроорганы, состоящие из эндокринных клеток, расположенных по всей протяженности паренхимы ПЖ, выполняющей экзокринные функции. Их основная масса локализуется в хвостовой части. Размер островков Лангерганса составляет 0,1—0,2 мм, общее их количество в ПЖ человека составляет от 200 тыс. до 1,8 млн.
Клетки образуют отдельные группы, между которыми проходят капиллярные сосуды. От железистого эпителия ацинусов они отграничены соединительнотканными и проходящими там же волокнами нервных клеток. Эти элементы нервной системы и клетки островка образуют нейроинсулярный комплекс.
Структурные элементы островков — гормоны — выполняют внутрисекреторные функции: регулируют углеводный, липидный обмен, процессы пищеварения, метаболизм. У ребенка в железе имеется 6% этих гормональных образований от общей площади органа. У взрослого человека эта часть ПЖ значительно уменьшена и составляет 2% от поверхности железы.
История открытия
Скопления клеток, отличающиеся по своему виду и морфологическому строению от основной ткани железы и располагающиеся небольшими группами преимущественно в хвосте ПЖ, впервые обнаружил в 1869 году немецкий патологоанатом Пауль Лангерганс (1849—1888 гг.).
В 1881 году выдающейся российской ученой, патофизиологом К.П. Улезко-Строгановой (1858—1943 гг.) были выполнены фундаментальные физиологические и гистологические работы по исследованию ПЖ. Результаты были опубликованы в журнале «Врач», 1883 г., № 21 – статья «О строении поджелудочной железы при условии ее покоя и деятельности». В ней она впервые в то время высказала гипотезу об эндокринной функции отдельных образований ПЖ.
На основании ее работ в 1889—1892 гг. в Германии О. Минковский и Д. Меринг установили, что при удалении ПЖ развивается сахарный диабет, который можно устранить, проведя подсадку части здоровой ПЖ под кожу прооперированному животному.
Отечественный ученый Л.В. Соболев (1876—1921 гг.) одним из первых на основании проведенных исследовательских работ показал значение островков, открытых Лангергансом и названных его именем, в продуцировании вещества, имеющего отношение к возникновению сахарного диабета.
В дальнейшем благодаря большому количеству исследований, проведенных физиологами в России и других странах, были открыты новые научные данные об инкреторной функции ПЖ. В 1990 г. впервые проведена трансплантация островков Лангерганса человеку.
Типы островковых клеток и их функции
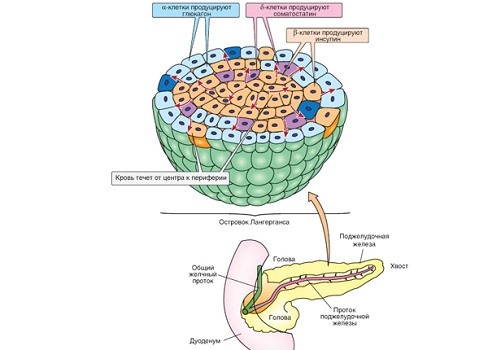
Клетки ОЛ отличаются морфологическим строением, выполняемыми функциями, локализацией. Внутри островков они имеют мозаичное расположение. Каждый островок имеет упорядоченную организацию. В центре находятся клетки, которые выделяют инсулин. По краям – периферийные клетки, количество которых зависит от размеров ОЛ. В отличие от ацинусов, ОЛ не содержит своих протоков – гормоны поступают сразу в кровь через капилляры.
Выделяют 5 основных видов клеток ОЛ. Каждый из них синтезирует определенный вид гормона, регулируя пищеварение, углеводный и белковый обмен:
- α-клетки,
- β-клетки,
- δ-клетки,
- РР-клетки,
- эпсилон-клетки.
Альфа-клетки
Альфа-клетки занимают четверть площади островка (25%), являются вторыми по значимости: вырабатывают глюкагон — антагонист инсулина. Он контролирует процесс расщепления липидов, способствует повышению уровня сахара в крови, участвует в снижении уровня кальция и фосфора в крови.
Бета-клетки
Бета-клетки составляют внутренний (центральный) слой дольки и являются основными (60%). Они отвечают за выработку инсулина и амилина — компаньона инсулина в регуляции глюкозы крови. Инсулин выполняет несколько функций в организме, главная — нормализация уровня сахара. Если нарушается его синтез, развивается сахарный диабет.
Дельта-клетки
Дельта-клетки (10%) образуют внешний слой в островке. Они продуцируют соматостатин — гормон, значительная часть которого синтезируется в гипоталамусе (структуре головного мозга), а также обнаруживается в желудке и кишечнике.
Функционально он тесно связан также с гипофизом, регулирует работу определенных гормонов, которые вырабатываются этим отделом, а также подавляет образование и выделение гормонально-активных пептидов и серотонина в желудке, кишечнике, печени и самой поджелудочной железе.
ПП-клетки
РР-клетки (5%) располагаются по периферии, их численность примерно составляет 1/20 части островка. Они могут секретировать вазоактивный интестинальный полипептид (ВИП), панкреатический полипептид (ПП). Максимальное количество ВИП (вазоинтенсивного пептида) встречается в пищеварительных органах и мочеполовой системе (в мочеиспускательном канале). Он влияет на состояние пищеварительного тракта, выполняет много функций, в том числе обладает спазмолитическими свойствами в отношении гладкой мускулатуры желчного пузыря и сфинктеров органов пищеварения.
Эпсилон-клетки
Самые редкие из входящих в состав ОЛ — эпсилон-клетки. При микроскопическом анализе препарата из дольки ПЖ можно определить, что их число от общего состава составляет меньше 1%. Клетки синтезируют грелин. К наиболее изученной среди его многочисленных функций относится возможность влиять на аппетит.
Какие патологии возникают в островковом аппарате?
Поражение клеток ОЛ приводит к тяжелым последствиям. При развитии аутоиммунного процесса и выработке антител (АТ) к клеткам ОЛ, количество всех перечисленных структурных элементов резко снижается. Поражение 90% клеток сопровождается резким уменьшением синтеза инсулина, что приводит к сахарному диабету. Выработка антител к островковым клеткам поджелудочной железы происходит в основном у людей молодого возраста.
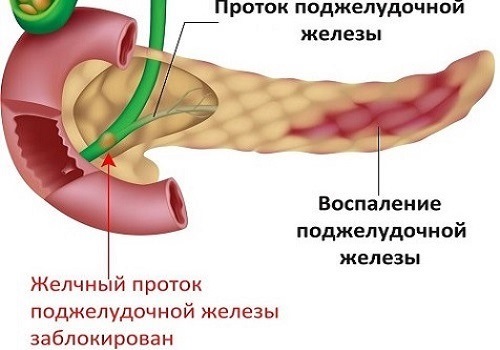
К серьезным последствиям в связи с повреждением островков приводит панкреатит — воспалительный процесс в тканях ПЖ. Нередко он протекает в тяжелой форме в виде панкреонекроза, при котором происходит тотальная гибель клеток органа.
Определение антител к островкам Лангерганса
Если в организме по каким-то причинам произошел сбой в организме, и началась активная выработка антител против собственных тканей, это приводит к трагичным последствиям. Когда воздействию антител подвергаются бета-клетки, развивается сахарный диабет I типа, связанный с недостаточной выработкой инсулина. Каждый вид образующихся антител действует против определенного вида белка. В случае с островками Лангерганса — это структуры бета-клеток, отвечающие за синтез инсулина. Процесс протекает прогрессивно, клетки полностью погибают, нарушается углеводный обмен и при нормальном питании больной может умереть от голода из-за необратимых изменений в органах.
Разработаны диагностические методы определения наличия антител к инсулину в организме человека. Показаниями к такому исследованию являются:
- ожирение с учетом семейного анамнеза,
- любая патология ПЖ, включая перенесенные травмы,
- тяжелые инфекции: в основном вирусные, которые могут стать толчком к развитию аутоиммунного процесса,
- тяжелые стрессы, психическое перенапряжение.
Существует 3 типа антител, благодаря которым диагностируется сахарный диабет I типа:
- к декарбоксилазе глутаминовой кислоты (одна из заменимых аминокислот в организме),
- к вырабатывающемуся инсулину,
- к клеткам ОЛ.
Это своеобразные специфические маркеры, которые необходимо включать в план обследования пациентов с имеющимися факторами риска. Из перечисленного объема исследований выявление антител к компоненту глутаминовой аминокислоты является ранним диагностическим признаком СД. Они появляются, когда клинические признаки болезни еще отсутствуют. Определяются в основном в молодом возрасте и могут быть использованы для выявления людей с предрасположенностью к развитию болезни.
Трансплантация островковых клеток
Трансплантация клеток ОЛ является альтернативой пересадке поджелудочной железы или ее части, а также установке искусственного органа. Связано это с высокой чувствительностью и нежностью тканей ПЖ к любым воздействиям: она легко травмируется и с трудом восстанавливает свои функции.
Пересадка островков сегодня дает возможность лечить сахарный диабет I типа в тех случаях, когда инсулинзамещающая терапия достигла пределов и становится малоэффективной. Метод впервые применен канадскими специалистами и заключается во введении пациенту при помощи катетера здоровых эндокринных донорских клеток в воротную вену печени. Он направлен на то, чтобы заставить работать и сохранившиеся собственные бета-клетки.
За счет функционирования пересаженных постепенно синтезируется необходимое для поддержания нормального уровня глюкозы крови количество инсулина. Эффект наступает быстро: при удачно проведенной операции через две недели состояние больного начинает улучшаться, заместительная терапия сходит на нет, ПЖ начинает самостоятельно синтезировать инсулин.
Опасность операции заключается в отторжении пересаженных клеток. Используются трупные материалы, которые тщательно подбираются по всем параметрам совместимости тканей. Поскольку таких критериев существует около 20, антитела, присутствующие в организме, могут привести к разрушению тканей поджелудочной железы. Поэтому важную роль играет правильное медикаментозное лечение, направленное на снижение иммунных реакций. Препараты подбираются таким образом, чтобы избирательно блокировать некоторые из них, влияющие на выработку антител, к клеткам пересаженных островков Лангерганса. Это позволяет до минимума снизить риск для поджелудочной железы.
На практике пересадка клеток ПЖ при сахарном диабете I типа показывает хорошие результаты: зафиксированных смертельных случаев после такой операции не отмечалось. Определенное количество больных значительно снизило дозу инсулина, а часть прооперированных пациентов перестала в нем нуждаться. Восстановились и другие нарушенные функции органа, улучшилось самочувствие. Значительная часть вернулась к нормальному образу жизни, что позволяет надеяться на дальнейший благоприятный прогноз.
Как и при пересадке других органов, операция на ПЖ, помимо отторжения, опасна другими побочными явлениями за счет нарушения разной степени секреторной деятельности поджелудочной железы. В тяжелых случаях это приводит:
- к панкреатическим поносам,
- к тошноте и рвоте,
- к выраженному обезвоживанию,
- к другим диспепсическим явлениям,
- к общему истощению.
После проведенной процедуры на протяжении всей жизни пациент должен непрерывно получать иммуносупрессорные препараты, чтобы предотвратить отторжение чужеродных клеток. Действие этих лекарств направлено на снижение иммунных реакций — выработку антител. В свою очередь, отсутствие иммунитета увеличивает риск развития любой, даже простой инфекции, которая может осложниться и вызвать серьезные последствия.
Продолжаются исследования по пересадке ПЖ от свиньи — ксенотрансплантация. Известно, что анатомия железы и свиной инсулин наиболее приближены к человеческим и отличаются от него одной аминокислотой. До открытия инсулина в лечении тяжелого сахарного диабета использовался экстракт из поджелудочной железы свиньи.
Зачем проводят пересадку?
Поврежденные ткани ПЖ не восстанавливаются. В случаях осложненного сахарного диабета, когда пациент находится на высоких дозах инсулина, такое оперативное вмешательство спасает больного, дает шанс на восстановление структуры бета-клеток. В ряде клинических исследований больным пересаживались эти клетки от доноров. В результате восстанавливалась регуляция углеводного обмена. Но притом пациентам приходится проводить мощную иммуносупрессивную терапию, чтобы не произошло отторжение донорских тканей.
Не всем пациентам с сахарным диабетом I типа показана трансплантация клеток. Существуют строгие показания:
- отсутствие результатов от применяемого консервативного лечения,
- резистентность к инсулину,
- выраженные метаболические нарушения в организме,
- тяжелые осложнения болезни.
Где проводят операцию и сколько стоит?
Процедуру замещения островков Лангерганса широко проводят в США — таким образом лечат диабет любого типа на ранних стадиях. Этим занимается один из институтов по диабетическим исследованиям в Майами. Полностью вылечить СД таким способом не удается, но достигается хороший терапевтический эффект, притом риски тяжелых осложнений сводятся к минимуму.
Цена такого вмешательства составляет порядка 100 тыс. $. Послеоперационная реабилитация и проведение иммунодепрессивной терапии составляет от 5 до 20 тыс. $. Стоимость этого лечения после проведения операции зависит от реакции организма на пересаженные клетки.
Практически сразу после проведенной манипуляции ПЖ начинает нормально функционировать самостоятельно, и постепенно ее работа улучшается. Процесс восстановления занимает примерно 2 месяца.
Профилактика: как сохранить островковый аппарат?
Так как функция островков Лангерганса поджелудочной железы − вырабатывать важные для человека вещества, то для сохранения здоровья этой части ПЖ необходима модификация образа жизни. Основные пункты:
- отказ от алкоголя и курения,
- исключение вредной пищи,
- физическая активность,
- сведение к минимуму острых стрессов и нервно-психических перегрузок.
Наибольший вред поджелудочной железе приносит алкоголь: он разрушает ткани ПЖ, приводит к панкреонекрозу — тотальной гибели всех видов клеток органа, которые восстановить невозможно.
К аналогичным последствиям приводит излишнее употребление жирной и жареной пищи, особенно если это происходит натощак и регулярно. Нагрузка на ПЖ значительно возрастает, количество ферментов, которые необходимы для переваривания большого количества жиров, увеличивается и истощает орган. Это приводит к фиброзу и изменениям в остальных клетках железы.
Поэтому при малейших признаках нарушения пищеварительных функций рекомендуется обратиться к гастроэнтерологу или терапевту с целью своевременной коррекции изменений и ранней профилактики осложнений.
Источник статьи: http://diabetsahar.ru/pankreatit/podzheludochnaya-zheleza/funkcii-i-patologiya-ostrovkov-langergansa-sboj-vydelyaemyx-gormonov.html
Изменение островкового аппарата поджелудочной железы
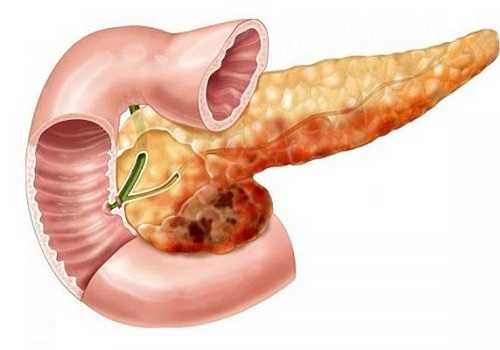
Опухоль поджелудочной железы симптомы и лечение. По своему происхождению новообразования в поджелудочной железе бывают доброкачественными или злокачественными.
Часто их выявляют после инструментального обследования других органов. На УЗИ однозначно вид опухоли не определить. При подозрении на новообразование в поджелудочной железе нужно обратиться к врачу, который назначит дополнительное всестороннее обследование.
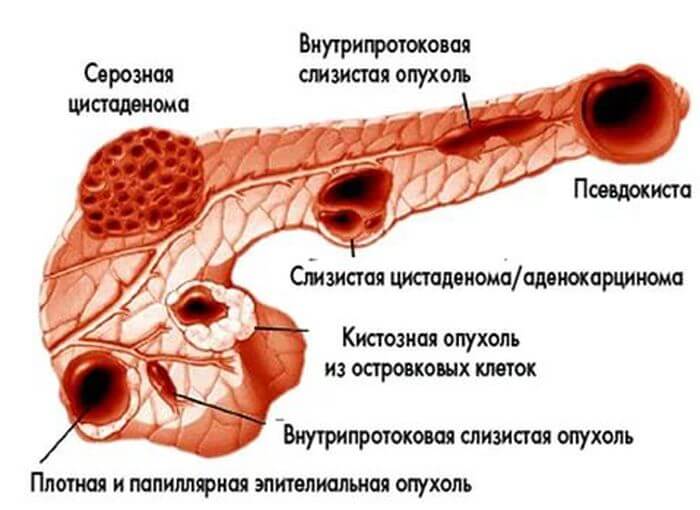
Классификация опухолей
Новообразование в поджелудочной железе разделяются:
По локализации — месту возникновения в структуре железы:
Гистологическому строению определяется, из каких клеток образовалась опухоль:
- эпителиальное происхождение;
- железистой паренхимы;
- из островкового эпителия;
- неэпителиального генеза;
- дизонтогенетические.
Функциональным нарушениям – состояние, связанное с изменением регуляции в организме: гормональной или нервной. Орган остается неповрежденным, но деятельность поджелудочной железы нарушается.
Симптомы
Развитие опухоли до поры протекает без видимых симптомов. Когда она разрастается и возможно прорастает в близлежащие органы: желудок, тогда появляются типичные симптомы, с которыми доктор знаком. По симптомам он назначает всестороннее обследование.
Злокачественная опухоль поджелудочной железы проявляет свои симптомы при значительном разрастании:
Закупорка протоков
Закупорке протоков (обтюрация) – появляется при сдавливании образованием органов, которые нарушают свое функционирование, и проявляется болями, свидетельствующими о том, что новообразование просочилось сквозь нервные окончания. У каждого пациент симптомы проявляются индивидуально и зависят от места возникновения.
Опухоль головки поджелудочной железы провоцирует боль в правом подреберье. Опухоль хвоста поджелудочной железы вызывает дискомфорт и боль в левом подреберье. Если образованием охвачено тело поджелудочной железы, то боль проявляется вкруговую, опоясывающая.
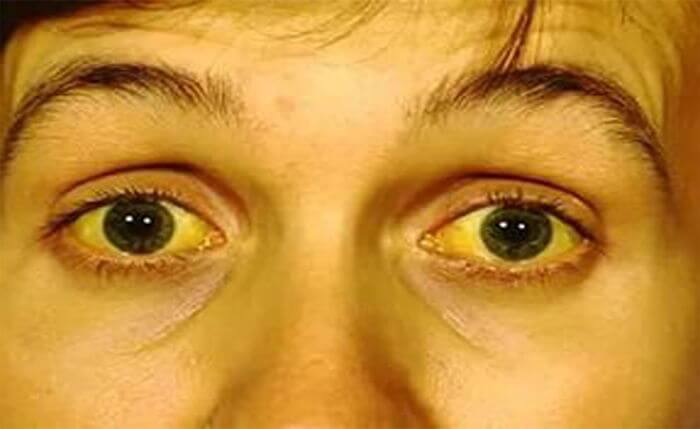
Боль сильно увеличивается при несоблюдении диеты, а также лежа на спине. Сдавливание органов приводит к закупорке желчных протоков, проявляющееся в оттоке желчи из печени в кишечник. Результатом становится механическая желтуха. У нее свои симптомы:
- желтушное окрашивание кожи, склер или слизистых оболочек;
- обесцвечивание стула;
- потемнение мочи;
- изменение размера печени и желчного пузыря в сторону увеличения;
- возникновение кожного зуда.
Рак поражает близлежащие органы, из которых может, в любой момент открыться кровотечение.
Интоксикация
Интоксикация организма. Ее признаки часто путают с признаками заболеваний и отклонений в ЖКТ. Симптомы похожи, но действие на организм интоксикации значительно тяжелее:
- резкое снижение веса;
- потеря аппетита;
- вялость, немощь, апатия;
- повышение температуры.
Доброкачественная опухоль поджелудочной железы позволяет классифицировать симптоматику 2 видов:
Ранняя стадия имеет бессимптомное течение, и приобретает их в процессе роста:
- боли вверху живота, подреберьях, правом или левом, отдающая в спину, усиливающаяся по ночам;
- дискомфорт и боль после приема пищи;
- постепенная потеря веса;
- тошнота, снижение аппетита, немощь и потеря трудоспособности.
Поздняя стадия – проявляется симптомами, как и при злокачественной опухоли. Помимо перечисленных выше, симптомов вызывает страх и нервные расстройства, повышает потоотделение. Симптомы могут возникать постепенно или внезапно. И они отличаются, завися от типа доброкачественного образования.
Риски возникновения
Точной причины появления раковых клеток нет. Но опухолевый процесс имеет свои факторы риска, о которых многие знают. Среди них:
- Вредные привычки: алкоголь, курение.
- Генная предрасположенность.
- Неправильное питание.
- Панкреатит.
- Неблагоприятная экологическая обстановка.
Диагностика
Всесторонне обследование пациента, используя различные методы исследования, позволит выяснить тяжесть опухоли: очаги, размеры, действие на соседние органы, метастазирование.
Обследование поможет определиться с методикой лечения:
- УЗИ. Позволяет увидеть новообразование, очаг его распространения.
- Компьютерная томография с введением контрастного вещества выявит не только очаги опухоли, но и метастазы, если они есть.
- Рентгенологические методы: А) Рентгенография определяет последствия прорастания опухоли на желудок и двенадцатиперстную кишку, сдавливание органов, диффузия слизистых оболочек, снижение моторики. В) Релаксационная дуоденография определяет локализацию опухоли и последствия ее разрастания. С) Ирригография выявляет дефекты в поперечно-ободочной кишке в результате прорастания опухоли.
- Эндоскопическая ретроградная холангиопанкреатография позволяет осмотреть желчную и панкреатическую системы с целью выявления их поражений. Взять материал для биопсии из неблагополучных очагов.
- Эндоскопический ультразвук. За счет технического оснащения: эндоскоп, видеокамера, ультразвуковой датчик, возможно, исследовать новообразование, введя инструменты через кишку. Такое исследование позволяет выявить новообразование на ранних стадиях.
- Рентгенохирургическая диагностика с контрастом позволяет выявить причины механической желтухи и смещение артерий.
- Радионуклидное исследование позволяет выявить закупорку общего с поджелудочной железой желчного протока.
- Нашумевший спорный тестер Джека Андраки, основан на анализе крови или мочи, используя специальную бумагу.
Главное в диагностике — установка медицинского диагноза на основании интерпретация полученных результатов исследования и анализов, формирование экспертного заключения.
Лечение
Необходимое лечение подбирается доктором на основании диагностики и анализов.
Хирургическая терапия всегда показана при обнаружении доброкачественного образования. Исследование гистологии со срезов образования позволит точно установить была ли она доброкачественной. Основные операции по удалению новообразований:
- Резекция состоит в удалении части поджелудочной железы, чаще в ее хвосте.
- Удаление непосредственно образования способом вылущивания. Выполняются для опухолей, которые продуцируют гормоны: доброкачественная инсулома.
- Панкреатодуоденальная резекция производится в случае размещения образования на головке железы. Оно удаляется вместе с 12-перстной кишкой.
- Селективная артериальная эмболизация закупоривает сосуд, на котором растет образование с целью отключить подпитку кровоснабжением. Используется при гемангиоме.
Химиотерапия
Химиотерапия призвана лечить злокачественное образование при помощи токсинов и ядов, которые называются химиопрепаратом. Она бывает: предоперационной, послеоперационной, профилактической, лечебной.
Поскольку раковые клетки бесконечно делятся, то химиотерапия циклично повторяется в расчете с клеточным циклом деления. Процедура состоит из капельного введения препарат или приёмом таблеток.
Наружная радиотерапия, являющаяся разновидностью терапии лучевой. Суть излечения — бомбардирование зоны новообразования излучением от медицинского ускорителя в виде пучка элементарных частиц. Проводится сеансами через фиксированный промежуток времени. Показания к применению:
- Сокращение размера опухоли на поджелудочной железе перед хирургическим вмешательством.
- Локально-возникшем раке поджелудочной железы.
- Уменьшение страданий при метастазах.
- Предотвращение рецидивов рака после хирургической операции.
Симптоматическая терапия направлена на снятие болей и облегчения страданий умирающего пациента: гормональная терапия – это лечение с помощью применения гормонов, способных тормозить рост рака. Продлевает продолжительность жизни.
Виротерапия применяет онкотропные или онколитические вирусы в терапевтических целях, мобилизуя против злокачественных клеток естественные защитные силы иммунной системы организма.
Нанонож как необратимая электропорация, разрушающая раковые клетки путем воздействия на них электрическим полем большой интенсивности локализовано. Для этого применяется специальный аппарат — нанонож.
В настоящее время слывет одним из самых результативных способов уничтожения опухоли в поджелудочной железе. Факт возможности повторения процедуры важное обстоятельство для повторного проведения при рецидивах или неоперабельном раке.
Шансы на выздоровление или жизнь после оперативного лечения
Сама операция на поджелудочной железе мало опасна. Прогноз оптимистичней при ранних сроках выполнения операции. Полностью выздоравливают пациенты с доброкачественными опухолями: глюкагономы, инсуломы, гастриномы и их разновидности
Рак поджелудочной железы имеет печальную статистику:
- На операцию поступают пациенты, у которых отсутствуют множественные метастазы, А это, как правило, лишь 15% больных. Для 85 % предоставляются виды лечения, направленные на продление жизни.
- Смертность на операционном столе у одного пациента из 6.
- Продолжительность жизни до 5 лет у каждого десятого больного после хирургического вмешательства, у остальных меньше.
После оперативного лечения возможны осложнения в функционировании организма. Любая операция влечет приспособление организма к потере органа или его части. Если орган жизненно важен, то адаптация проходит тяжелее. У пациентов после удаления опухоли поджелудочной железы, симптомы и лечение влекут 2 проблемы: сбои при пищеварении, снижение инсулина в организме.
Решаются проблемы дефицита путем назначения медикаментозных препаратов. При сопутствующих удалениях частей близлежащих органов: желудка, селезенки, двенадцатиперстной кишки врач посоветует надлежащую терапию и диету.
Профилактика
Поскольку ученые неутомимо работают над вопросом изучения причин, дающих толчок развитию рака, а ответа на них нет со 100 % достоверностью, поэтому руководства во избежание заболевания нет.
Лучший способ профилактики исключить знакомые всем факторы риска. Быть внимательным к себе при проявлениях болей в месте расположения железы. Не откладывать визит к доктору и хотя бы поверхностное обследование УЗИ.
Опухоль поджелудочной железы симптомы и лечение животрепещущая тема для многих страдающих заболеванием.
Источник статьи: http://clinica-opora.ru/%D1%82%D0%B5%D1%80%D0%B0%D0%BF%D0%B8%D1%8F/%D0%BF%D1%80%D0%B8%D0%B3%D0%BE%D0%B2%D0%BE%D1%80-%D0%BB%D0%B8-%D0%BE%D0%BF%D1%83%D1%85%D0%BE%D0%BB%D1%8C-%D0%BF%D0%BE%D0%B4%D0%B6%D0%B5%D0%BB%D1%83%D0%B4%D0%BE%D1%87%D0%BD%D0%BE%D0%B9-%D0%B6%D0%B5/
Заболевания островкового аппарата поджелудочной железы | Часть 1.
Содержание:
Описание
↑ Сахарный диабет
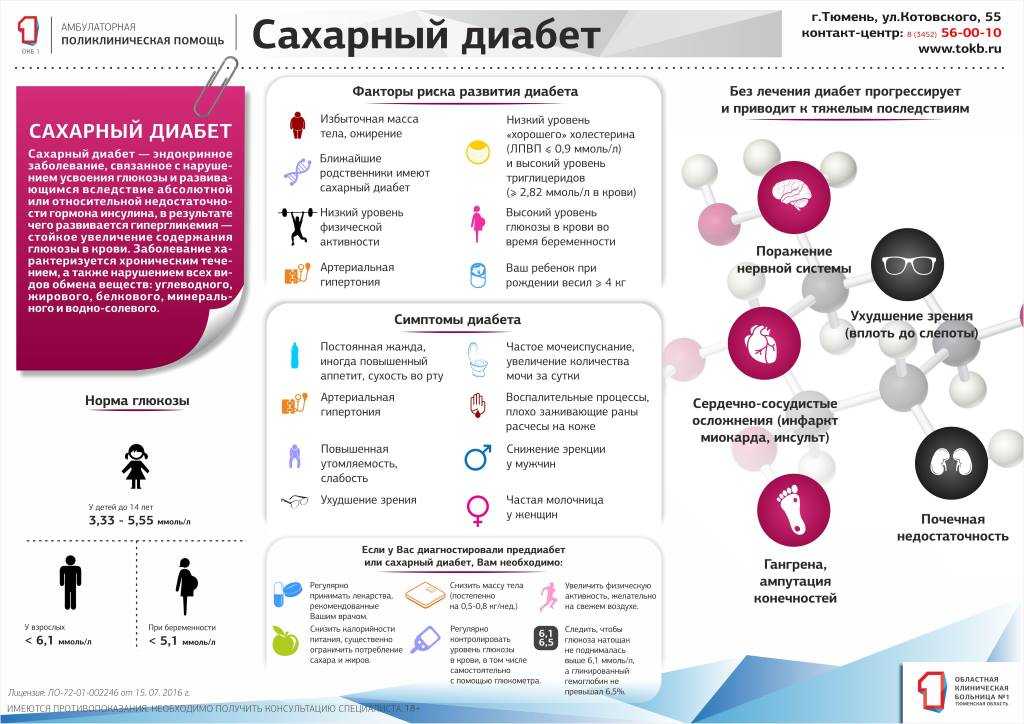
Сахарный диабет — одно из самых распространенных эндокринных заболеваний. Заболеваемость сахарным диабетом из года в год увеличивается во всех странах мира.
Рассматривают генетически обусловленный и генетически не обусловленный сахарный диабет. По данным различных авторов, наследственный характер сахарного диабета отмечается в 5—55% случаев. Однако вопрос о том, наследуется ли при этом недостаточность b-клеток островкового аппарата поджелудочной железы или недостаточная активность инсулина на периферии — еще не решен. Существует мнение, что если оба родителя больны сахарным диабетом, вероятность заболевания детей равна 100%, если болен один из родителей — 50%, если болен брат или сестра 25%.
Если сахарный диабет наследственный, то все монозиготные близнецы, являются конкордантными (при выявлении заболевания у одного из них, оно выявляется и у другого); у дизиготных близнецов это наблюдается реже.
Сахарный диабет наследуется как по доминантному, так и по рецессивному типу. К факторам риска относятся: переедание в течение длительного времени, ожирение, беременность (особенно осложненная), травмы, инфекции, интоксикации, некоторые эндокринные заболевания (диффузный токсический зоб, болезнь Иценко—Кушинга, феохромоцитома, акромегалия и др.).
В развитии сахарного диабета основную роль играет инсулиновая недостаточность. Последняя может быть абсолютной и относительной. Абсолютная инсулиновая недостаточность обусловлена нарушением синтеза и секреции инсулина, в результате чего содержание его в крови уменьшается. При относительной инсулиновой недостаточности существенных изменений в синтезе и секреции инсулина не отмечается. Содержание его в крови обычно нормальное, а иногда даже повышенное. Относительная инсулиновая недостаточность обусловлена впепанкреатическимн факторами.
Связывание инсулина с белком, в результате чего он переходит в малоактивную форму, — одна из причин, имеющая наибольшее значение в развитии сахарного диабета.
Возникновение сахарного диабета может быть обусловлено контринсулярными факторами — гормональными антагонистами инсулина. К ним относятся соматотропный гормон, адренокортикотронный гормон, глюкокортикоиды, адреналин, глюкагон, йодсодержащие тиреоидные гормоны. Нужно отметить, что данные гормоны на некоторых этапах обмена веществ действуют как синергисты, но их контринсулярное действие значительно сильнее.
Известно, какое значение в развитии сахарного диабета имеют и негормональные антагонисты инсулина. К ним относятся антитела, которые образуются при введении гетерогенного инсулина. Другим антагонистом является, по-видимому, липопротеид, который был обнаружен при аллоксановом диабете у экспериментальных животных и у людей во время гипогликемического шока. Антагонистическим действием обладает и вещество, выявленное у экспериментальных животных и у больных сахарным диабетом с инсулинорезистентностью, при диабетической коме оно связано с a-фракцией белков сыворотки крови. Особое внимание уделяется антагонисту, связанному с альбуминами крови — синальбумину. Этот антагонист находят как у здоровых, так и у больных сахарным диабетом и у их родственников, но у последних содержание его значительно выше, что рассматривается как один из признаков наследственного предрасположения к сахарному диабету.
При сахарном диабете нарушается углеводный, белковый и жировой обмен. Вследствие ослабления гликолиза и усиления неогликогенеза возникает гипергликемия. Нарушается доставка глюкозы в ткани, так как для прохождения ее через клеточные мембраны необходим инсулин, снижается и потребление глюкозы тканями.
Инсулиновая недостаточность снижает интенсивность жирового обмена. Уменьшается синтез жира в печени, мышцах и жировой ткани, а липолиз значительно усиливается, и в кровь поступает большое количество неэстерифицированных жирных кислот (НЭЖК). Отмечается избыточное образование кетоновых тел, гиперхолестеринемия.
Инсулиновая недостаточность влечет за собой нарушение белкового обмена, тормозится синтез белка, а это приводит к уменьшению количества альбуминов, увеличению содержания а2-глобулпнов (диспротеинемпи) и парапротеинемпи. В результате нарушения синтеза белка уменьшается образование антител и понижается иммунобиологическая реактивность организма больных сахарным диабетом. Нарушается обмен липопротеидов, гликопротеидов, снижается синтез мукополисахаридов. Инсулиновая недостаточность вызывает также нарушения водного и минерального обмена.
Основные клинические проявления сахарного диабета — гипергликемия и глюкозурия. При этом заболевании наблюдаются различные изменения в органах и тканях, особенно часто поражается сердечно-сосудистая система.
Классификаций сахарного диабета предложено очень много. Для их унификации эксперты ВОЗ предложили рассматривать следующие стадии этого заболевания: потенциальный диабет, латентный диабет, асимптоматический диабет, клинический диабет.
По классификации, предложенной Институтом экспериментальной эндокринологии и химии гормонов АМН СССР, различают три стадии: потенциальный диабет, или предрасположенность к диабету, латентный диабет и явный диабет.
По тяжести сахарный диабет определяют как легкий, средней тяжести и тяжелый. В основе такого деления лежат клинические данные, уровень гликемии, наличие или отсутствие кетоза, реакции на различные антидиабетические средства.
Из всех эндокринных расстройств сахарный диабет наиболее часто вызывает изменения со стороны органа зрения. Наиболее тяжелое поражение — диабетическая ретинопатия.
Благодаря успехам в лечении сахарного диабета в настоящее время длительность жизни больных с этим заболеванием значительно увеличилась. Однако в связи с тем, что длительность течения сахарного диабета имеет большое значение при возникновении изменений в глазах, они стали встречаться чаще. Как причина слепоты заболевания глаз, связанные с сахарным диабетом, по данным современных авторов, составляют 10% среди всех возрастных групп и 20% среди людей в возрасте 45—74 лет [Khan S., Hiller J., 1974]. Приводятся данные о том, что вероятность слепоты для больных сахарным диабетом старше 50 лет в 20 раз больше, чем для людей, не страдающих этим заболеванием.
Нередко глазные симптомы при сахарном диабете дают возможность оценить общее состояние больного, например резкая гипотония глаз при диабетической коме, временные зрительные расстройства при гипогликемической коме. Иногда характерные для сахарного диабета патологические изменения органа зрения дают основание предположить у больного заболевание сахарным диабетом, что в ряде случаев после проведения соответствующих исследований подтверждается. Нами из 2000 случаев заболеваний глаз впервые выявлен сахарный диабет в 2,25%. При исследовании крови у 706 больных старческой катарактой установлена гипергликемия в 14,3% [Марголис М. Г. и др., 1967].
Рассмотрим вопрос об изменении придатков глаза и глазного яблока при сахарном диабете.
↑ Изменения век и конъюнктивы
У больных сахарным диабетом имеется склонность к заболеваниям кожных покровов, что обусловлено пониженной сопротивляемостью к инфекции и сенсибилизацией организма к различным эндогенным и экзогенным факторам. Часто у таких больных возникают блефариты, блефароконъюнктивиты, мейбомит, халазионы, ячмени, экзема кожи век и др. Эти заболевания имеют более длительное течение, чем обычно, и часто дают рецидивы. Сахарный диабет при всех указанных болезнях является отягощающим фактором.
При сахарном диабете наблюдаются подкожные и подконъюнктивальные кровоизлияния, варикозные расширения конъюнктивальных сосудов, микроаневризмы. Отмечаются и дистрофические изменения — ксантелазмы, представляющие собой плоские образования соломенно-желтого цвета. Они локализуются чаще у внутреннего угла глазной щели как на верхнем, так и на нижнем веке и очень медленно увеличиваются. Ксантелазмы обусловлены отложением холестерина, холинэстеров.
У больных с диабетом встречаются и заболевания конъюнктивы воспалительного характера (конъюнктивиты). Каких-либо характерных признаков, свойственных сахарному диабету, они не имеют.
↑ Изменения сосудистой оболочки глазного яблока
При сахарном диабете в сосудистой оболочке глазного яблока наблюдаются как воспалительные, так и дистрофические изменения. Воспалительный процесс в увеальном тракте может возникнуть в результате инфекционного, а также токсико-аллергического воздействия. К токсико-аллергическим заболеваниям относятся воспаления переднего отдела сосудистой оболочки при сахарном диабете — ириты и иридоциклиты, которые чаще бывают двусторонними.
Ирит редко протекает изолированно. Это обусловлено тем, что и радужная оболочка, и цилиарное тело имеют общее кровоснабжение; кроме того, радужная оболочка непосредственно переходит в цилиарное тело.
Иридоциклит бывает острым или хроническим. При остром течении отмечаются резкая боль в глазу, слезотечение, светобоязнь, иногда блефароспазм, может быть и головная боль. Появляется перикорнеальная или смешанная инъекция, иногда наблюдается отек (хемоз) конъюнктивы вокруг роговой оболочки. Изменяется цвет радужной оболочки, рисунок ее становится стушеванным. Влага передней камеры глазного яблока мутнеет вследствие проникновения в нее клеточных элементов, фибрина; зрачок суживается. Реакции зрачков становятся вялыми, что обусловлено, так же как и сужение зрачков, тем, что ткань радужной оболочки пропитывается серозной жидкостью и форменными элементами. Особенно сильные боли наблюдаются при воспалительном процессе в цилиарном теле во время пальпации глазного яблока в этой области. Для циклита характерно также появление на задней поверхности роговой оболочки преципитатов, экссудата в стекловидном теле.
Воспалительный выпот при диабетическом ирите или иридоциклите обычно фибринозного характера, что сопровождается появлением желатинозного экссудата, гипопиона. Экссудат обычно рассасывается быстро, задние синехии под воздействием лечения разрываются довольно легко. Однако может возникнуть и помутнение стекловидного тела, развиться помутнение хрусталика. Собственно сосудистая оболочка, как правило, в процесс не вовлекается. Таким образом, течение диабетического ирита, иридоциклита в большинстве случаев бывает доброкачественным.
Ирит, иридоциклит у больных сахарным диабетом может возникнуть так же, как и у лиц, не страдающих данным заболеванием, в связи с туберкулезом, ревматизмом, сифилисом и др. В таких случаях сахарный диабет является отягощающим фактором. Многие авторы отмечают, что ирит, иридоциклит могут возникнуть при разной степени гипегликемии и глюкозурии, причем на течение процесса это существенного влияния не оказывает.
В послеоперационном периоде (после полостных глазных операций), если больных оперируют в состоянии некомпенсированного сахарного диабета и если не применяют профилактически бактерицидные и бактериостатичеокие средства, осложнения (ирит, иридоциклит, кровоизлияние в переднюю камеру) наблюдаются чаще, чем у лиц, не страдающих сахарным диабетом.
Сосудистые и дистрофические изменения в радужной оболочке и цилиарном теле при сахарном диабете встречаются довольно часто. Методом флюоресцентной ангиографии можно выявить ранние изменения сосудов в радужной оболочке. В. Friedberg с соавт. (1973) различают три степени иридопатии. При I степени отмечаются ограниченный выход флюоресцеина в поздних стадиях ангиографин; при II — неравномерное распределение флюоресцеина у папиллярного края и при III степени наблюдается массивный выход красителя в строму радужной оболочки. У здоровых людей флюоресцеин из сосудов не просачивается. Выявлена корреляция между длительностью заболевания сахарным диабетом и сосудистыми изменениями в радужной оболочке, а также между выраженностью иридопатии и ретинопатии.
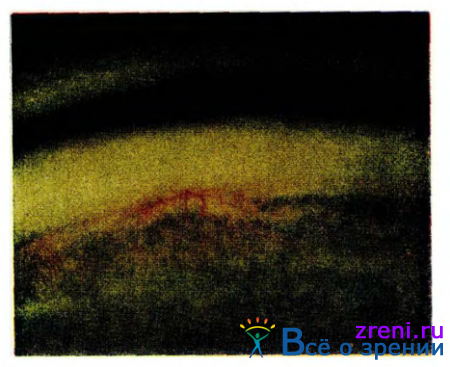
Рубеоз радужной оболочки (рис. 44)
встречается в 4—6% случаев заболеваний, чаще у женщин. Новообразованные сосуды появляются между пигментной каймой зрачка и сфинктером радужной оболочки и постепенно распространяются на периферию, радужки и иридо-корнеальный угол. Позднее развивается атрофия стромы радужной оболочки. Новообразованные сосуды могут быть источником кровотечения при глазных полостных операциях. Позднее образуются гониосинехпи в иридо-корнеальном углу (см. рис. 65).
Массивная синехиальная облитерация дренажной зоны может вести к повышению внутриглазного давления с развитием вторичной глаукомы. Считают, что геморрагическая глаукома почти всегда возникает при рубеозе радужной оболочки и протекает остро или подостро [Francois J., 1972]. Рубеозу радуяшой оболочки нередко сопутствует пролиферирующая диабетическая ретинопатия.
На происхождение рубеоза радужной оболочки существуют разные точки зрения. Согласно одной из них, изменения в радужной оболочке развиваются вследствие сосудистой недостаточности и дистрофических изменений. Имеется «воспалительная» теория, а также мнение о том, что пролиферация сосудов возникает вследствие воздействия специфических химических факторов.
При биомикроскопическом и гониоскопическом исследовании дистрофические изменения радужной оболочки и патология иридокорнеального угла выявляются нередко. Последнее выражается в экзогенной пигментации, иногда развиваются гониосинехпи [Шульпина Н. Б., Марголис М. Г., 1971, и др.].
При гистологическом исследовании глаз больных сахарным диабетом после энуклеации наблюдаются отек и набухание пигментного эпителия радужной оболочки и цилиарного тела, разрыхление их.
Дистрофические изменения радужной оболочки, а особенно новообразование сосудов (рубеоз), встречаются преимущественно при длительном течении сахарного диабета.
Патологические изменения собственно сосудистой оболочки — хориоидеи, у больных сахарным диабетом возникают в сочетании с изменениями сетчатой оболочки — ретинопатиями. Изолированных поражений ее обычно не отмечается.
↑ Изменения хрусталика
Хрусталик имеет своеобразное строение и с возрастом претерпевает определенные изменения. В результате деления клеток однослойного эпителия образуются новые хрусталиковые волокна, старые волокна теряют воду, становятся плотными и оттесняются к центру. Этот процесс длится почти всю жизнь. В результате уплотнения хрусталиковых волокон формируется ядро, которое окружено кортикальным слоем и капсулой и к 40—45 годам становится плотным. В связи с тем, что ядро постепенно увеличивается, кортикальный слой уменьшается, и хрусталик становится менее эластичным. Наряду с этим изменяется и его химический состав.
В хрусталике содержится до 65 % воды (в капсуле меньше, чем в кортикальном слое), около 30% белков. Кроме того, в его состав входят неорганические соединения. Хрусталик не имеет кровоснабжения; он получает питание из омывающей его внутриглазной жидкости, что обеспечивается проницаемостью капсулы хрусталика. Следует отметить то обстоятельство, что капсула хрусталика имеет отрицательный заряд, поэтому через нее легче проникают положительно заряженные коллоиды. Как и другие тканевые мембраны, капсула хрусталика имеет так называемую направленную проницаемость. Так, проницаемость для ряда веществ снаружи внутрь больше или меньше проницаемости изнутри кнаружи. Например, для глюкозы и аскорбиновой кислоты она больше в направлении снаружи внутрь. Соотношение различных ионов оказывает большое влияние на проницаемость капсулы хрусталика и, следовательно, на его питание.
Главным источником энергии хрусталика является гликолиз (расщепление глюкозы). В хрусталике содержится 52 мг% глюкозы, причем при гипергликемии содержание глюкозы увеличивается, а при гипогликемии уменьшается. Существенную роль в энергетическом обмене играют фосфорные соединения.
В окислительно-восстановительных процессах хрусталика участвуют глутатион и аскорбиновая кислота. Глутатион состоит из 3 аминокислот: глутаминовой, гликоколя и цистеина (сульфгидрильная группа цистеина обеспечивает окислительно-восстановительные процессы). В хрусталике имеются липиды (лецитин, холестерин), но в меньшем количестве, чем в других тканях.
Патологические изменения хрусталика в основном выражаются в помутнениях — в развитии катаракты. Различают две основные группы катаракт: врожденные и приобретенные. Мы рассмотрим катаракты второй группы: старческую, диабетическую и осложненную.
Старческая катаракта относится к прогрессирующим катарактам. В начальной стадии ее вблизи экватора хрусталика появляются помутнения в виде радиальных линий или секторообразных полос, обращенных основанием к экватору, а вершиной — к полюсу хрусталика. Иногда помутнения появляются субкапсулярно в форме тонкой скорлупки (чашевидная катаракта). Гораздо реже помутнения начинаются в ядре хрусталика или в ближайших к нему кортикальных слоях (ядерная катаракта). Понижение зрения при начальной кортикальной катаракте незначительное, и оно может долго сохраняться высоким, тогда как при ядерной катаракте зрение нарушается рано.
Ранним проявлением начинающейся катаракты может быть возникновение близорукости (иногда значительной) в связи с оводнением хрусталика, которое усиливает его преломляющую силу.
Начальные помутнения хрусталика могут долгое время оставаться стабильными, но все же через некоторое время процесс прогрессирует и наступает II стадия — незрелой, иногда набухающей катаракты. Помутнения увеличиваются, сливаются между собой, постепенно закрывая область зрачка. В результате набухания помутневших хрусталиковых волокон объем хрусталика увеличивается, передняя камера становится мельче. Острота зрения снижается, при значительном набухании хрусталика может повышаться внутриглазное давление. Третья стадия, зрелой катаракты, характеризуется равномерным помутнением всего хрусталика. Вследствие уменьшения его объема в связи с потерей воды передняя камера углубляется. Область зрачка приобретает равномерный серый цвет, острота зрения падает до светоощущения. Четвертая стадия — перезрелой катаракты — развивается в результате дистрофических изменений. Вследствие потери воды помутневшие кортикальные слои сморщиваются, ядро может опускаться книзу. Передняя камера становится глубокой, возникает дрожание радужной оболочки. В капсуле хрусталика в результате разрастания клеток эпителия образуются блестящие белые бляшки, в кортикальном слое наблюдаются отложения холестерина, извести.
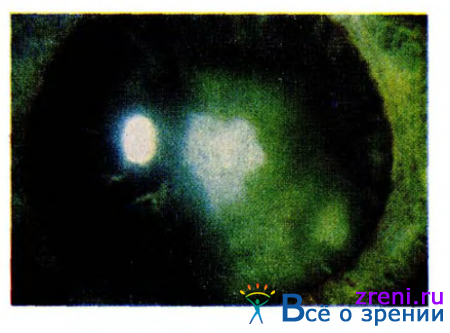
Специфическая диабетическая катаракта, обусловленная сахарным диабетом, в настоящее время встречается редко в связи с тем, что в большинстве случаев лечение больных сахарным диабетом начинается своевременно. Для диабетической, обычно двусторонней, катаракты характерно возникновение ее в молодом возрасте, быстрое прогрессирование. Считают, что помутнение хрусталика у больных молодого возраста свидетельствует о тяжелом течении сахарного диабета. Связь развития катаракты с сахарным диабетом бывает наиболее отчетливой именно у молодых людей в отличие от больных пожилого и старческого возраста, особенно в случаях развитой катаракты (рис. 45).
В ранних стадиях развития диабетическая катаракта имеет при биомикроскопии характерный вид. Помутнения возникают преимущественно в суб эпителиальных поверхностных кортикальных слоях хрусталика под передней и задней капсулами, волокна хрусталика раздвигаются водяными щелями, отмечаются обилие вакуолей, стушеванность оптических зон раздела. Под задней капсулой хрусталика помутнения могут сливаться между собой, образуя блюдцеобразное помутнение. Диабетическая катаракта нередко сочетается с воспалительным процессом в радужной оболочке, цилиарном теле, но клинические проявления ее бывают незначительными. Гистологическая картина диабетической катаракты напоминает таковую при субкапсулярной корковой катаракте.
Осложненные катаракты возникают ири воспалительных процессах в сосудистом тракте (в том числе при диабетических иритах и иридоциклитах), близорукости, глаукоме и др. Если осложненная катаракта возникла не в результате воспалительного процесса, вызванного сахарным диабетом, последний все же оказывает известное влияние на ее течение.
Необходимо отметить, что старческая катаракта у больных сахарным диабетом развивается чаще и в более молодом возрасте. Следует указать и на то, что катаракта может быть и смешанного типа, с элементами старческих и диабетических изменений.
Данные о распространении катаракты у больных сахарным диабетом неоднозначны; ее частота колеблется от 16,5 до 62,8% [Марголис М. Г., 1972]. По данным М. Г. Марголиса и Н. Б. Шульпиной (1967), на основании биомикроскопических исследований у больных сахарным диабетом приобретенные изменения хрусталика установлены в 82% случаев, в том числе классическая диабетическая катаракта в 2%. У 19% больных помутнения по локализации и клинической картине можно было расценивать как изменения, свойственные диабетичской катаракте (но утверждать это с полной категоричностью, конечно, нельзя). Интересно отметить, что из 18% больных, у которых не было обнаружено изменений хрусталика, у 15 % лечение проводили инсулипом и только у 3 % другими препаратами.
Существуют различные теории патогенеза старческой катаракты. Развитие катаракты связывают с нарушением проницаемости капсулы хрусталика. В частности, установлено, что инсулин понижает проницаемость капсулы хрусталика для аскорбиновой кислоты. Известную роль в патогенезе старческой катаракты отводят нарушению липидного обмена. Исследования М. Г. Марголиса и соавт. (1970) уровня холестерина в крови у больных старческой
катарактой в известной мере подтверждают мнение, что нарушение липидного обмена является одним из патогенетических факторов старческой катаракты: по суммарным данным, среди 1295 больных старческой катарактой гиперхолестеринемия отмечена у 44,1%.
В происхождении старческой, а также и диабетической катаракт большое значение придают нарушению углеводного обмена, что влечет за собой понижение активности энергетических процессов в хрусталике.
В известной мере подтверждают справедливость этого взгляда данные о частоте гипергликемии при старческой катаракте. По данным некоторых авторов, она достигает 30% [Примаков Ф. Д., 1965]. Нами установлена гипергликемия у 14,3% больных со старческой катарактой. Имеется мнение, что развитие диабетической катаракты обусловлено непосредственной инсулярной недостаточностью.
Существовавший ранее взгляд, что катаракта при сахарном диабете развивается в связи с увеличением содержания сахара во влаге передней камеры и в стекловидном теле, не оправдался. Дело в том, что увеличение уровня сахара во внутриглазных жидкостях при сахарном диабете очень незначительно и такая концентрация сахара не может вызвать помутнение хрусталика. Экспериментально удается вызвать помутнение хрусталика при гораздо более высокой концентрации сахара в жидкостях, в которых он находится.
Анализ наших исследований позволяет высказать следующие соображения. Возникновение изменений хрусталика, по-видимому, является одним из ранних проявлений сахарного диабета. При длительном течении этого заболевания, тяжелой его форме, наличии изменений глазного дна, свойственных сахарному диабету, изменений хрусталика может и не быть, если больные своевременно начали получать инсулин. Непосредственная инсулярная недостаточность, возможно, является одним из моментов, вызывающих изменения хрусталика.
↑ Изменения стекловидного тела
Изменения стекловидного тела в основном выражаются в появлении в нем помутнений, кровоизлияний. При сахарном диабете они встречаются несколько чаще, чем обычно, а некоторые виды помутнений являются специфическими для данного заболевания.
Летающие мушки могут быть физиологическим явлением, обусловленным наличием в стекловидном теле эмбриональных клеток блуждающих лейкоцитов или связаны с метаболическими нарушениями.
Помутнения стекловидного тела встречаются в виде хлопьев, нитей, пленок, а иногда могут быть диффузными. Иногда помутнения стекловидного тела бывают прикреплены тонкими нитями к диску зрительного нерва или к сетчатой оболочке. Такие изменения хорошо выявляются при биомикроскопии. Помутнения стекловидного тела могут возникнуть в результате воспалительного процесса в сосудистом тракте, при высокой близорукости, а также в результате дистрофических изменений (разжижение стекловидного тела), возникающих от различных причин (местный воспалительный процесс в глазу, атеросклероз, метаболические нарушения, сахарный диабет и др.) Помутнения стекловидного тела могут полностью рассасываться, но могут организоваться в соединительнотканные тяжи, при этом возможна отслойка сетчатой оболочки.
Представляют интерес встречающиеся в стекловидном теле так называемые астероидные тельца. В разжиженном стекловидном теле появляются множественные подвижные мелкие помутнения белого цвета, острота зрения при этом не снижается. Помутнения наблюдаются в таком большом количестве, что становится затруднительным офтальмоскопическое исследование. Астероидные тельца в 70—75% случаев встречаются только в одном глазу, обычно в старческом возрасте, одинаково часто как у мужчин, так у женщин. Возникновение астероидных телец связывают с сахарным диабетом. Отмечено, что у лиц с астероидными тельцами в стекловидном теле сахарный диабет встречается в 5 раз чаще, чем у лиц с прозрачным стекловидным телом. При исследовании содержания холестерина в крови у больных, у которых диагностированы астероидные тельца в стекловидном теле, установлено, что средний уровень его был равен 313%, содержание жиров и фосфолипидов находилось в соответствии с уровнем холестерина [Bard L. А., 1964].
Кровоизлияния в стекловидное тело могут возникнуть в результате местного процесса в глазу, травмы, а также в результате общих причин (атеросклероз, артериальная гипертония и др.) и могут сопровождаться понижением остроты зрения. Кровоизлияния в стекловидное тело определяются при исследовании в проходящем свете в виде темных образований; иногда кровь заполняет все стекловидное тело (гемофтальм). В таких случаях наступает резкое понижение остроты зрения, иногда до потери светоощущения.
При сахарном диабете кровоизлияния в стекловидное тело могут сочетаться с поражением сетчатой оболочки (ретинопатия).Известно, что наиболее тяжелое течение диабетической ретинопатии наблюдается в тех случаях, когда она сопровождается кровоизлияниями в стекловидное тело.
Кровоизлияния в стекловидное тело при сахарном диабете рассасываются очень медленно, часто организуются, что может повлечь за собой отслойку сетчатой оболочки.
Продолжение в следующей статье: Заболевания островкового аппарата поджелудочной железы | Часть 2.
Источник статьи: http://zreni.ru/articles/disease/1438-zabolevaniya-ostrovkovogo-apparata-podzheludochnoy-zhelezy-chast-1.html