Опухоль поджелудочной железы — симптомы и лечение
Что такое опухоль поджелудочной железы? Причины возникновения, диагностику и методы лечения разберем в статье доктора Пылева А. Л., онколога со стажем в 20 лет.
Определение болезни. Причины заболевания
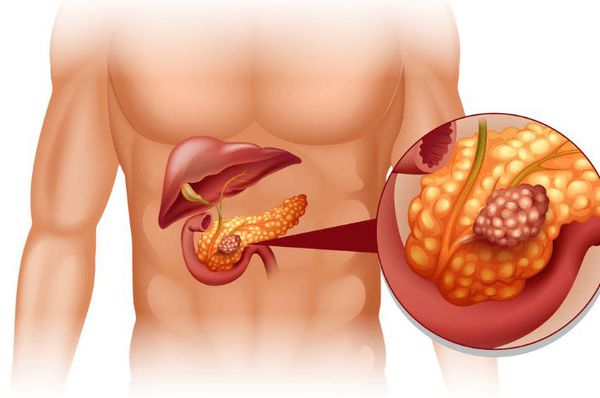
Опухоли поджелудочной железы (ПЖ) — это новообразования, которые произрастают из островковых (железистых) клеток органа, а также из эпителия, который выстилает панкреатические протоки.
В абсолютном большинстве случаев (около 95 %) это экзокринные опухоли злокачественной природы (аденокарцинома панкреатических протоков), т. е. рак [1] . Экзокринными называют опухоли, произрастающие из экзокринной части поджелудочной железы, которая составляет около 97 % её массы. Эта часть железы продуцирует панкреатические ферменты, выделяемые в просвет 12-перстной кишки.
Помимо экзокринной, есть еще эндокринная часть, которая представлена панкреатическими островками (островками Лангерганса). Функция эндокринной части заключается в выработке некоторых гормонов, например инсулина и глюкогана, которые поддерживают необходимый уровень глюкозы в крови.
Рак поджелудочной железы — это одно из самых сложных онкологических заболеваний, поскольку на начальном этапе оно протекает бессимптомно, а при развитии клинической картины опухоль уже является инкурабельной (неизлечимой). Однако, даже если новообразование диагностировано на ранней стадии, радикальное лечение всё равно провести очень сложно, поскольку железа располагается глубоко в брюшной полости и удаление опухоли требует особой квалификации хирургической бригады. Кроме того, такие операции сопряжены с высоким риском серьёзных осложнений (кровотечения, некрозы, перитонит, сепсис ), которые могут привести к преждевременной гибели пациента.
Показатели заболеваемости и смертности от рака ПЖ практически одинаковы, то есть количество заболевших за год приблизительно равно числу умерших. Это связывают с невозможностью прижизненной диагностики предраковых изменений, сложностью выявления заболевания на ранней стадии, низкой эффективностью лечения [1] .
В России в 2015 году среди всех онкологических заболеваний рак поджелудочной железы составлял 3,3 %. Абсолютное число новых случаев в 2015 году насчитывало 8791 среди мужского населения и 8924 среди женского населения. Средний возраст заболевших мужчин — 64,6 года, женщин — 70,3 года. За прошлое десятилетие показатели заболеваемости раком поджелудочной железы среди мужчин выросли на 9,39 %, среди женщин — на 14,95 %. Смертность от рака ПЖ в 2015 году в России составляла 5, 9 %, что соответствует пятому месту после рака лёгкого, желудка, ободочной кишки и молочной железы [3] .
Причины заболевания
Причины развития опухолей поджелудочной железы до конца не ясны. В настоящее время приходится говорить о факторах риска, при наличии которых вероятность образования такой патологии возрастает [2] .
- Курение табака. У 1-2 % курильщиков развивается рак поджелудочной железы. В целом считается, что курение увеличивает вероятность развития такой опухоли в 2 раза, и у каждого четвёртого курильщика причиной развития рака стал табак. Естественно, чем больше стаж и чем интенсивнее курение, тем выше риски [2] .
- Особенности диеты. Существует гипотеза, что избыток в рационе мяса, жиров животного происхождения, а также недостаток свежих овощей могут спровоцировать развитие опухолей ПЖ, однако на сегодняшний день достоверных данных, подтверждающих или опровергающих эту гипотезу, нет.
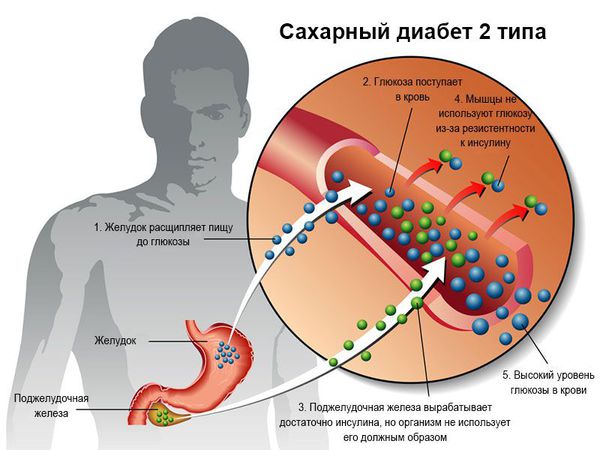
- Сахарный диабет (СД) 2 типа. Это заболевание рассматривается в качестве основного фактора риска развития рака ПЖ. Например, обширный мета-анализ, включающий 36 исследований, проведённых на 9220 больных, показал, что при СД 2 типа риски развития рака ПЖ выше на 60 % по сравнению с общей популяцией [12][13][14] .
- Хронический панкреатит. Все виды хронического панкреатита увеличивают вероятность развития опухолей ПЖ в 20 раз, за исключением наследственного хронического панкреатита, который увеличивает относительные риски в 50 раз [13] .
- Инфекционные заболевания. Есть данные, свидетельствующие о высоком уровне заболеваемости раком ПЖ в популяциях людей с высоким распространением гастродуоденитов (воспалительных заболеваний слизистой оболочки желудка и 12-перстной кишки), возникших на фоне персистирующей (протекающей длительное время) хеликобактерной инфекции.
- Наследственная предрасположенность. Считается, что около 5 % рака ПЖ носит семейный характер. При наличии одного случая рака ПЖ в семье, вероятность его развития у других родственников повышается в 2-3 раза, при заболевании двух родственников первой линии родства — в 6 раз.
- Ожирение тоже является фактором риска развития опухоли поджелудочной железы. В России чуть чаще болеют женщины, но если брать мировую статистику, достоверных различий нет.
Причина образования гормональных и негормональных опухолей фактически одна — мутация в клетках. В норме такие клетки должны уничтожаться, но при раке этого по разным причинам не происходит, клетки быстро размножаются и формируется опухоль.
Симптомы опухоли поджелудочной железы
Как уже было сказано, симптомы опухолей поджелудочной железы на ранних стадиях отсутствуют. Первые признаки возникают только тогда, когда новообразование достигает больших размеров, сдавливает окружающие ткани или прорастает в них.
Выделяют общие симптомы, которые характерны для поражения ПЖ в целом, и специфические признаки, которые развиваются при локализации опухоли в конкретном отделе органа или при развитии специфических гормон-продуцирующих новообразований (инсулинома, гастринома, випома и др.).
Общие признаки [5] :
- Боль в эпигастрии может отдавать в спину. Выраженность боли может изменяться от незначительных болевых ощущений до сильных, нестерпимых приступов. Спровоцировать её возникновение может погрешность в диете (жирная пища, приём алкоголя), изменение положения тела (усиление болевых ощущений в положении лежа на спине). Многие принимают болезненность за симптом панкреатита или другие проблемы с поджелудочной железой. При этом уходит время, и заболевание неуклонно прогрессирует.
- Похудение. Снижение массы тела обусловлено нарушением пищеварительной функции, в частности всасывания жиров, что объясняется недостаточной продукцией соответствующих ферментов.
- Сахарный диабет. При раке ПЖ может развиться вторичный сахарный диабет, обусловленный поражением эндокринных клеток железы. При этом пациента может беспокоить жажда и повышение аппетита, а в биохимическом анализе крови будет определяться характерное повышение уровня глюкозы.
- Снижение аппетита, вплоть до отвращения к некоторым продуктам. Чаще всего это касается мяса и жирных «тяжёлых» блюд.
- Нарушение стула. Обычно больных беспокоит диарея, связанная с нарушением пищеварения из-за ферментной недостаточности.
- Тромбозы. В ряде случаев первичными проявлениями рака поджелудочной железы являются тромбозы глубоких вен нижних конечностей. При этом отмечается боль, отёчность ноги, локальное покраснение и увеличение температуры поражённой области.
- Симптомы интоксикации. Проявляются вялостью, апатией, повышением температуры тела, отвращением к некоторым продуктам. Эти симптомы связаны с системным токсическим действием опухоли и продуктов её распада на организм.
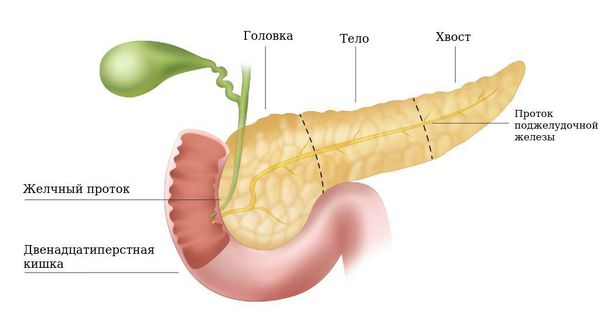
Симптомы, характерные для рака головки поджелудочной железы:
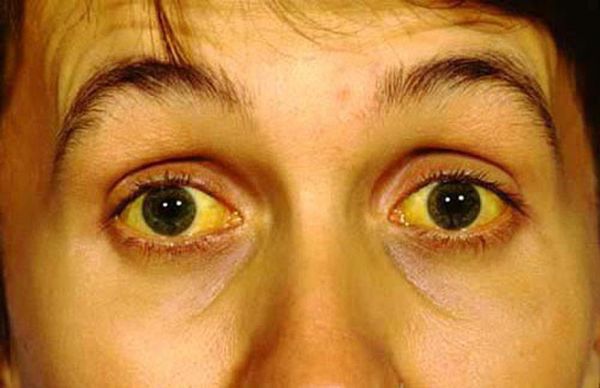
- Механическая желтуха. При раке головки поджелудочной железы опухоль сдавливает желчевыводящие протоки, что приводит к нарушению оттока желчи и развитию механической желтухи. Если вовремя не устранить обструкцию, состояние больного станет критичным и даже может закончиться летальным исходом.
- Рвота. Развивается в результате сдавления опухолью 12-перстной кишки.
Симптомы рака тела и хвоста поджелудочной железы:
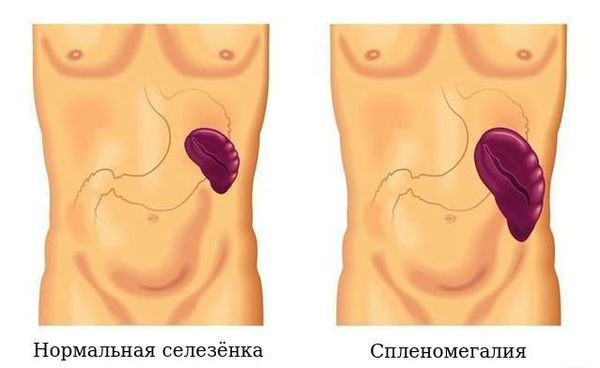
- Спленомегалия (увеличение селезёнки).
- Портальная гипертензия. Проявляется расширением вен пищевода и желудка, а также высоким риском кровотечения.
Симптомы эндокринных опухолей ПЖ [6] :
- Инсулиномы — опухоли β-клеток. В избыточном количестве секретируют гормон инсулин, который снижает концентрацию глюкозы в крови. Инсулиномы приводят к стойкой гипогликемии (пониженному уровню глюкозы в крови).
- Гастриномы — опухоли G-клеток. В избыточных количествах вырабатывают гормон гастрин, который стимулирует выработку желудочного сока. Гастриномы проявляются синдромом Золлингена — Эллисона, для которого характерна повышенная секреция желудочного сока, множественные язвы, стойкое нарастание симптоматики, не поддающейся коррекции медикаментозными препаратами.
- Випомы (панкреатическая холера) — опухоли D1-клеток. Вырабатывают избыточное количество вазоактивного интестинального полипептида, который снижает выработку соляной кислоты в желудке. Випомы проявляются хронической диареей, снижением уровня калия в крови, ахлоргидрией (отсутствием свободной соляной кислоты в полости желудка).
Патогенез опухоли поджелудочной железы
Чаще всего опухолью поджелудочной железы оказывается внутрипротоковая аденокарцинома. Процесс её образования многоступенчатый и предполагает прохождение определённых этапов морфологических изменений, которые описываются термином панкреатическая интраэпителиальная неоплазия (PanIN) [11] .
Выделяют следующие виды неоплазии протоков:
- PanIN 1А — нет признаков атипических изменений (изменений внешнего вида клетки, её формы, размера).
- PanIN 1В — нормальный по строению эпителий, в котором встречаются сосочковые образования.
- PanIN 2 — в эпителии помимо сосочков имеются признаки клеточной атипии.
- PanIN 3 — рак in situ (начальная стадия роста злокачественной опухоли).
Следует отметить, что протоковую дисплазию (неправильное развитие) очень сложно обнаружить, и она крайне редко диагностируется при жизни.
Еще до начала морфологических изменений в клетках происходят генетические мутации. Наиболее ранними событиями являются мутации в генах K-ras и активация генов EGFR и HER-2/neu, которые приводят к стимуляции различных внутриклеточных эффекторов. В конце концов это приводит к неконтролируемой пролиферации (размножению клеток) и развитию внутрипротоковой аденокарциномы.
Классификация и стадии развития опухоли поджелудочной железы
В зависимости от степени дифференцировки клеток все опухоли ПЖ делятся на доброкачественные и злокачественные.
По гистологическому варианту:
- Протоковая карцинома (опухоль эпителиального происхождения, развивающаяся из клеток, выстилающих протоки поджелудочной железы). Это наиболее часто встречающийся вариант рака ПЖ. На его долю приходится более 90 % всех случаев рака поджелудочной железы.
- Нейроэндокринные опухоли — это новообразования, которые развиваются из эндокринных клеток железы, находящихся в островках Лангерганса. Сюда относят инсулиномы, глюкагономы и др.
- Ацинарные опухоли — развиваются из клеток, продуцирующих ферменты. К данной категории относятся, например, випомы.
В зависимости от локализации выделяют следующие виды опухолей:
- Опухоли головки поджелудочной железы. Это излюбленное место локализации протоковых карцином. В частности, около 75 % таких образований располагаются именно в головке. Их размеры могут быть небольшими – около 2,5-3,5 см, но из-за близкого расположения к желчному протоку они могут приводить к его сдавлению и развитию желтухи.
- Опухоли тела поджелудочной железы. По распространённости занимают второе место.
- Опухоли хвоста поджелудочной железы — очень редкая локализация, встречается менее чем у 7 % больных.
- Тотальное поражение поджелудочной железы.
При раке поджелудочной железы, в зависимости от распространённости процесса, выделяют 4 стадии:
- Опухоль ограничена железой. Её размер составляет не более 2 см в наибольшем измерении.
- Опухоль не более 2 см, имеются признаки поражения лимфатических узлов, либо опухоль более 2 см, не выходящая за пределы железы, и без признаков метастазов.
- Опухоль до 2 см с поражением двух лимфатических узлов, либо более 2 см, не выходящая за пределы железы, с поражением одного лимфатического узла.
- Опухоль распространяется за пределы поджелудочной железы, без признаков метастазов, либо опухоль любого размера с поражением трёх и более лимфатических узлов, либо наличие отдалённых метастазов во внутренних органах [7] .
Осложнения опухоли поджелудочной железы
Чаще всего опухоли ПЖ начинают проявляться именно с осложнений:
- Механическая желтуха. Это наиболее частое осложнение для опухолей головки ПЖ. Оно обусловлено сдавлением желчевыводящего протока. При этом возникает ряд характерных симптомов: пожелтение кожи, потемнение мочи, светлый кал, симптомы интоксикации, кожный зуд. Если вовремя не наладить желчеотведение, это чревато очень тяжёлыми последствиями, вплоть до гибели пациента. Поэтому лечение всегда начинают с купирования желтухи, и только после стабилизации состояния больного планируют радикальное лечение, если оно возможно [3] .
- Кишечная непроходимость , которая формируется из-за сдавления опухолью просвета тонкого кишечника. П роявляется симптомами интоксикации, рвотой, общей слабостью, дегидратацией и др.
- Кровотечение и распад опухоли. Проявляются рвотой цвета кофейной гущи, дёгтеобразным калом, быстро нарастающей анемией.
- Гормон-продуцирующие опухоли приводят к развитию «гормональных бурь» (увеличения концентрации одного или нескольких гормонов с развитием соответствующей симптоматики), к оторые не поддаются медикаментозной коррекции.
Диагностика опухоли поджелудочной железы
Выявить опухоль ПЖ на ранних стадиях очень сложно ввиду анатомических и топографических особенностей органа. Как правило, прицельный диагностический поиск начинают уже после развития симптоматики. Следует учитывать, что она неспецифична и аналогичные признаки могут присутствовать и при других патологиях (холецистите, гепатите, панкреатите, гастродуодените).
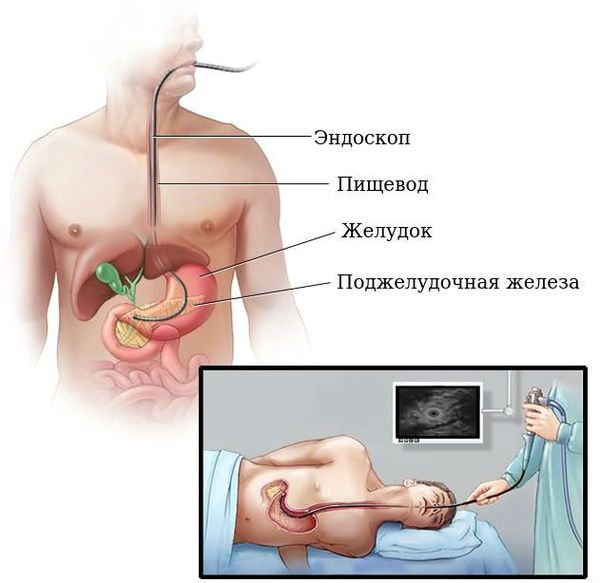
Наиболее простым и доступным методом обнаружения рака ПЖ является УЗИ брюшной полости и забрюшинного пространства. Более чувствительным методом является эндосонография, во время которой УЗИ датчик вводят в 12-перстную кишку. Это позволяет максимально приблизиться к поджелудочной железе и получить более чёткую и подробную картину.
Чаще всего в клинической практике используются следующие методы [8] :
- КТ и МРТ. Эти методы применяются не только для диагностики, но и для уточнения стадии заболевания и планирования хирургического лечения. С их помощью определяют размеры новообразования, его соотношение с окружающими тканями, наличие отдалённых и регионарных метастазов.
- Холангиопанкреатография. Данное исследование необходимо для того, чтобы оценить проходимость панкреатического и общего желчного протоков, может быть выполнено несколькими методами: панкреатография — рентгенологическое исследование железы после контрастирования её протока рентгеноконтрастным веществом. Экскреторная панкреатография — контраст вводится внутривенно и с током крови достигает поджелудочной железы. Затем вводится специальный препарат, усиливающий секреторную функцию поджелудочной железы, и когда она начинает секретировать контраст внутрь протоков, проводят серию снимков.
- Морфологическое исследование опухолевой ткани. Только после гистологического исследования возможно подтвердить диагноз. Чтобы его провести, выполняется биопсия — изъятие кусочка опухолевой ткани.
- Ангиография — это метод контрастного исследования кровеносных сосудов. И сследование необходимо для определения тактики лечения. В частности оно позволяет спланировать проведение радикальной операции.
- ПЭТ-КТ — позитронно-эмиссионная томография. Проводится с использованием радиофармпрепарата, является очень чувствительным методом, позволяющим с высокой точностью оценить распространённость опухолевого процесса.
- Лабораторные исследования. Перед началом лечения проводят определение онкомаркеров РЭА и СА9-19. У некоторых пациентов уровень этих белков изначально повышен, и при успешном лечении он снижается. Повторный подъём определяется при развитии рецидива или при прогрессировании заболевания [1] .
На первой стадии диагностики может быть достаточно КТ и лабораторного обследования, а при наличии у доктора вопросов относительно резектабельности новообразования может назначаться и МРТ, и ПЭТ, и ангиография. Любые хирургические манипуляции заканчиваются гистологическим заключением — именно оно подтверждает диагноз.
Лечение опухоли поджелудочной железы
Первым этапом при планировании лечения опухолей поджелудочной железы является определение морфологического варианта рака и его резектабельности. При местно-распространённом процессе помимо стандартного хирургического вмешательства может использоваться кибер-нож, нано-нож, стереотаксическая лучевая терапия, протонная терапия и др.
Протоковые опухоли, как правило, требуют обширных резекций с удалением всех вовлечённых в процесс тканей. Частичное удаление такого вида рака нецелесообразно ввиду его быстрого роста и прогрессирования. А вот при непротоковом раке объём операции может быть уменьшен. В некоторых случаях допускается частичная резекция опухоли и даже её полное удаление (энуклеация).
В первую очередь, возможность радикального хирургического удаления протоковой опухоли зависит от её взаимоотношения с крупными кровеносными сосудами, располагающимися в данной области. Если опухоль резектабельна, лечение начинают с операции, в остальных случаях на первом этапе показана химиотерапия (возможно в комбинации с лучевой терапией). После нескольких курсов проводят повторное исследование. Если опухоль хорошо отреагировала на лечение (произошло уменьшение её размера), вопрос о хирургическом вмешательстве решается повторно.
В связи с тем, что большинство пациентов с опухолями поджелудочной железы, как правило, преклонного возраста, лечение данной патологии всегда представляет сложную задачу [9] .
Хирургическое лечение
Как и в абсолютном большинстве случаев злокачественных новообразований внутренних органов, единственным методом радикального удаления первичной опухоли поджелудочной железы является хирургическое вмешательство. Учитывая то, что обычно диагноз выставляется на распространённых стадиях заболевания, операции носят обширный характер и требуют частичной резекции смежных органов [10] :
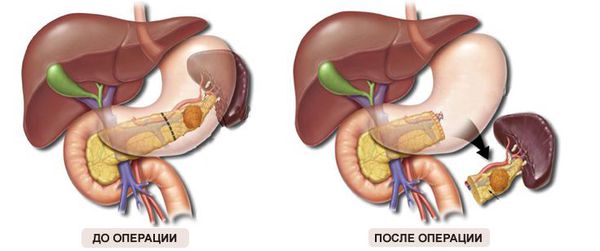
- При расположении рака в головке поджелудочной железы проводят не только удаление головки, а также выполняют резекцию желудка, желчных протоков, 12-перстной кишки и части тонкой кишки.
- При локализации рака в теле или хвосте ПЖ удаляют всю железу единым блоком с вовлечёнными в процесс тканями. Селезёнку пытаются сохранить, но если это невозможно, её тоже удаляют. Технически эта операция проще, чем резекция головки поджелудочной железы, но после тотального удаления органа такие пациенты вынуждены принимать пожизненную заместительную инсулинотерапию и ферменты.
Учитывая большой объём операций, после них требуется пластика, которая направлена на восстановление проходимости пищеварительной системы и желчевыводящих путей. После неё обязательно проводится многокурсовая химиотерапия по схеме FOLFIRINOX. Необходимость комбинированного лечения обусловлена следующими причинами:
- В большинстве случаев рак ПЖ представлен протоковой аденокарциномой, которую необходимо расценивать как первично-генерализованный процесс, т. е. на момент постановки диагноза есть основания предполагать наличие отдалённых микрометастазов.
- Причиной смерти после радикального удаления опухоли являются именно отдалённые метастазы.
Химиотерапия
Химиотерапия при протоковой карциноме не предотвращает ни развитие рецидива, ни рост метастазов, но она увеличивает период безрецидивной выживаемости, на какое-то время сдерживая генерализацию процесса [4] .
При условно нерезектабельном раке первым этапом лечения является химиотерапия (если нет желтухи, в противном случае проводят паллиативные операции по желчеотведению).
Преимуществ у такой тактики несколько. Во-первых, во время лечения определяется группа больных с неблагоприятным прогнозом, у которых уже на фоне проведения химиотерапии начинается прогрессирование. В этом случае дальнейшая операция нецелесообразна. Во-вторых, дооперационная химиотерапия позволяет системно воздействовать на организм, уничтожая микрометастазы. Это благоприятно сказывается на продолжительности жизни и качестве лечения. В-третьих, предоперационную терапию можно проводить практически всем больным. В то же время после обширных операций последующее лечение невозможно у четверти больных ввиду ухудшения их состояния и развития осложнений.
Ввиду того, что рак ПЖ часто диагностируется на поздних стадиях, встает вопрос об оказании паллиативной помощи таким больным (паллиативная помощь подразумевает улучшение качества жизни пациента с неизлечимым заболеванием). Ключевым моментом на этом этапе может стать желчеотведение. С этой целью проводятся несколько видов операций:
- Наложение обходных анастомозов — в обход опухоли формируется искусственный «путь», по которому желчь из печени будет попадать в тонкий кишечник. Это довольно травматичная и устаревшая методика, но в отдельных случаях (если опухоль «непроходима» или в конкретной клинике другие операции не выполняются в силу различных причин) она может быть вариантом выбора.
- Стентирование желчных протоков — в просвет протока в месте его компрессии устанавливается стент, который будет поддерживать его проходимость.
- Чрескожное чреспечёночное дренирование протоков — желчь выводится наружу с помощью дренажа, который устанавливается выше места обструкции желчевыводящих протоков.
Прогноз. Профилактика
Прогноз заболевания в первую очередь определяется гистологическим вариантом опухоли. Наиболее неблагоприятная ситуация при протоковой карциноме. Пятилетняя выживаемость у таких пациентов составляет менее 40 %, несмотря на агрессивно проведённое лечение. Другие формы рака имеют более благоприятное течение. Даже при четвёртой стадии до 70 % пациентов переживают пятилетний рубеж [2] .
Специфических мер профилактики рака поджелудочной железы не существует. В основном мнения специалистов сходятся на необходимости отказа от курения, соблюдении принципов рационального питания и снижении употребления алкоголя. Это позволяет предотвратить развитие и рецидив хронического панкреатита, который, в свою очередь, является одним из факторов риска развития рака поджелудочной железы [2] .
Источник статьи: http://probolezny.ru/opuhol-podzheludochnoy-zhelezy/
Интраэпителиальная неоплазия поджелудочной железы
Протоковая аденокарцинома — опухоль эпителиального происхождения, развивающаяся из клеток, выстилающих протоки поджелудочной железы. Процесс может затрагивать любую часть железы, но наиболее частой локализацией служит ее головка. Это одно из наиболее распространенных онкологических заболеваний поджелудочной железы. Опухоль чрезвычайно злокачественна и в большинстве случаев приводит к летальному исходу. Ежегодно в США заболевает 44 000 человек, 38 000 погибает. Тенденция такова, что протоковая аденокарцинома в своей летальности вскоре может опередить смертность от рака груди и толстой кишки.
Чаще всего данное заболевание встречается в промежутке между 55 и 84 годами. Особую роль играет наследственная предрасположенность: риск заболеть возрастает на 40% у людей, имеющих трех и более родственников первой линии, двух — на 10% и на 6% при наличии одного такого родственника. Табакокурение, частое употребление алкоголя, хронический панкреатит, ожирение так же предрасполагают к этому заболеванию. Имеются данные о связи с сахарным диабетом II типа и инфицированием Helicobacter pylori.
Считается, что аденокарцинома в своем развитии имеет некоторую стадийность. Всё начинается с преинвазивной стадии — панкреатической интраэпителиальной неоплазии. Это поражение эпителия стимулируется накоплением генетических мутаций. Наиболее распространенной является мутация в онкогене K-ras (встречается в 90% случаев). Другими часто встречающимися нарушениями служат мутация в Her-2 и потеря антионкогенных свойств p16, p53 и SMAD4.
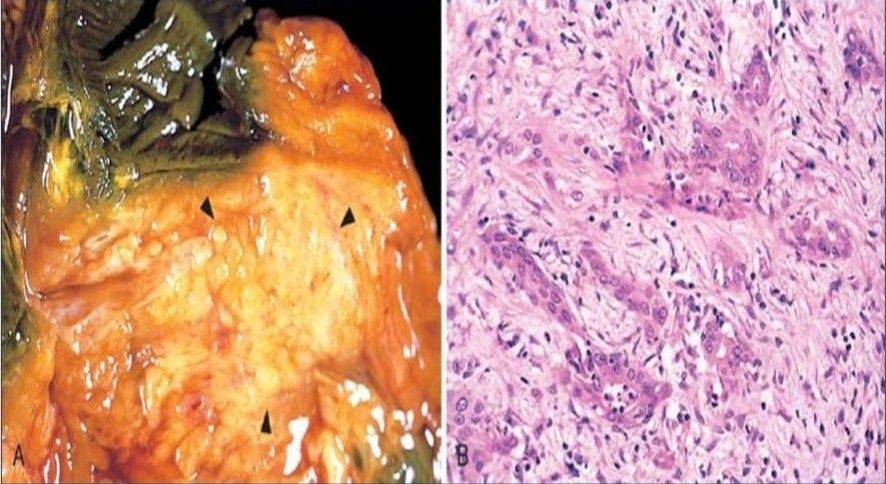
Макроскопически опухоль выглядит как неоднородная, склерозированная, грубая бело-желтая масса. Границы карциномы нечеткие, опухоль инфильтрирует окружающие ткани. Микроскопически практически во всех случаях определяется периневральная инвазия. Присутствуют сосудистые и лимфатические микрометастазы; часто обнаруживается некроз опухоли. Даже в тех случаях, когда аденокарцинома локализована, она имеет низкую степень дифференцировки, и ее очень сложно обнаружить на ранних, курабельных стадиях.
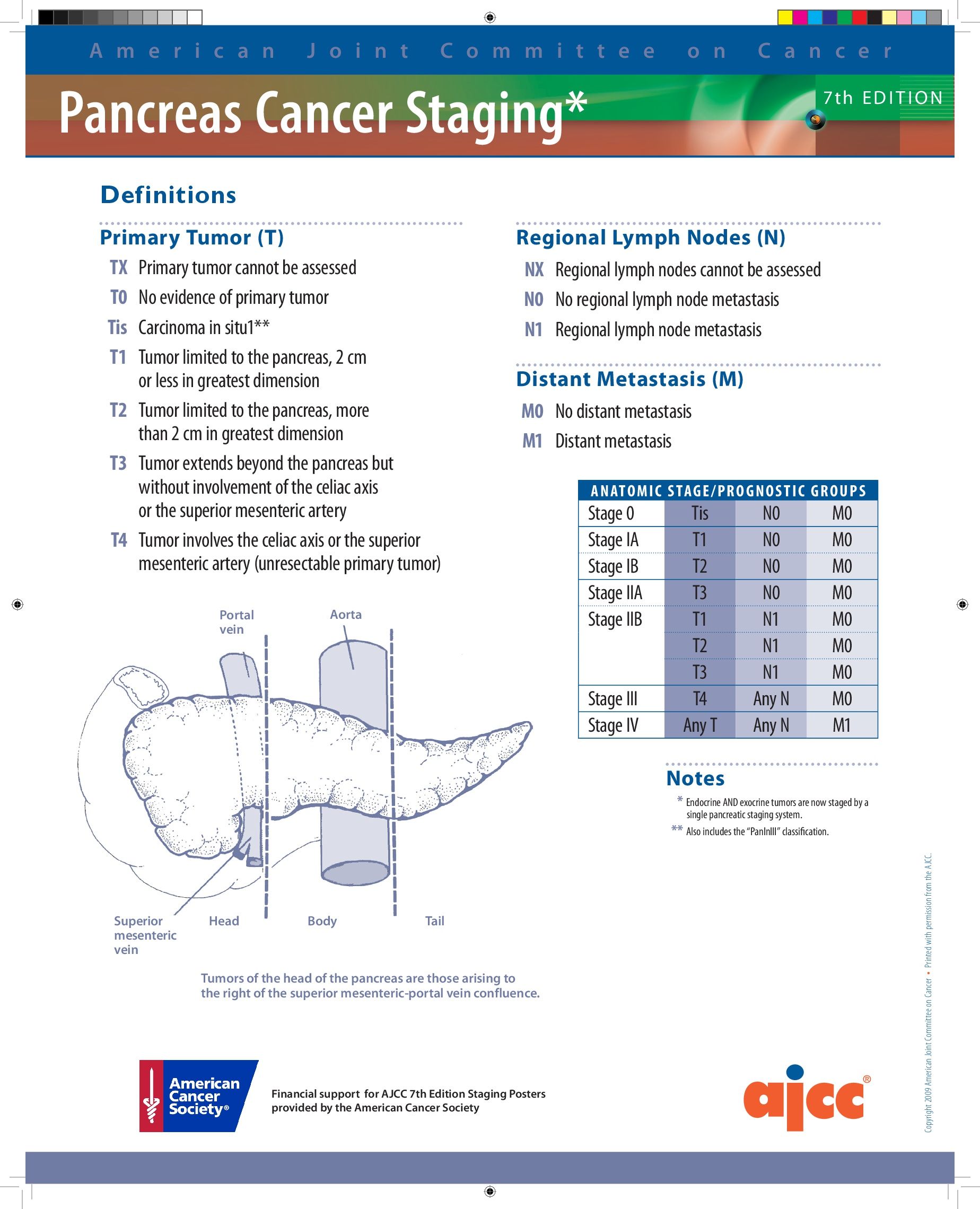
Рисунок 1 | Классификация рака поджелудочной железы по TNM.
TX: Невозможно оценить состояние первичной опухоли
T0: Отсутствуют признаки рака в поджелудочной железе
Tis: Самые начальные проявления рака без распространения опухоли — карцинома in situ
T1: Диаметр опухоли 2 см и менее, находится в пределах поджелудочной железы
T2: Диаметр опухоли более 2 см, находится в пределах поджелудочной железы
T3: Опухоль выходит за пределы поджелудочной железы, но в крупные артерии или вены рядом с органом не проникает
T4: Опухоль выходит за пределы поджелудочной железы и проникает в крупные артерии или вены рядом с органом. Опухоль категории T4 неоперабельна.
NX: Невозможно оценить cостояние регионарных лимфатических узлов.
N0: Отсутствуют признаки рака в регионарных лимфатических узлах.
N1: Опухоль распространяется на регионарные лимфатические узлы.
MX: Невозможно обнаружить отдаленные метастазы.
M0: Опухоль не метастазирует.
M1: В отдаленных органах выявляются метастазы. Рак поджелудочной железы метастазирует преимущественно в печень, легкие и на брюшину.
Стромальный компонент — опухолевое микроокружение — занимает около 70% всей массы опухоли. Строма слабо васкуляризована и обладает высоким интерстициальным давлением. Тем самым данные условия ведут к доминированию наиболее устойчивых, наиболее агрессивных субклонов. Эти субклоны резистентны к химиотерапии и хорошо адаптированы к экстремальным условиям. Таким образом, строма создает мощный барьер для эффективной лекарственной доставки и обеспечивает опухолевым клеткам стимулирующую среду.
Манифестация клинических симптомов происходит на более поздних стадиях, когда вероятность эффективного хирургического лечения составляет лишь 20%. Характер проявлений зависит от локализации патологического процесса. Как говорилось выше, наиболее часто поражается головка поджелудочной железы — в 60-70% случаев. Этой локализации присущи симптомы обтурации общего желчного протока: механическая желтуха, сопровождающаяся кожным зудом; ахоличный кал, темная моча. Присутствует и болевой синдром. В остальных случаях, при поражении тела и хвоста патогномоничным симптомом является наличие болей и потеря веса. Иногда аденокарцинома дебютирует как острый панкреатит. Среди общих симптомов также встречаются астения, анорексия, тошнота, рвота, диарея.
При подозрении на аденокарциному поджелудочной железы всем пациентам назначают исследование печеночного профиля. Маркером аденокарциномы служит CA 19-9, который повышается в 75-85% случаев, однако он недостаточно специфичен и не дает основания для постановки точного диагноза. Тем не менее, повышение данного маркера свидетельствует о рецидиве заболевания после оперативного лечения.
Золотым стандартом среди инструментальных методов исследования является компьютерная томография. Помимо этого диагностической ценностью обладают магнитно-резонансная холангиопанкреатография, эндоскопическая ретроградная холангиопанкреатография, абдоминальное УЗИ, чрескожная чреспечёночная холангиография, эзофагогастродуоденоскопия. Целью исследований является выяснение степени распространения опухоли, инвазии в окружающие ткани, наличия метастазов. По поводу биопсии ведутся споры: считается, что вмешиваться нужно, если возникла обтурационная желтуха, либо в том случае, когда опухоль достигла существенных размеров или дала распространенные метастазы. В таком случае биопсия нужна для определения тактики химиотерапии.
Терапия аденокарциномы поджелудочной железы проводится комплексно. Наиболее обнадеживающим является хирургическое лечение. К сожалению, на момент выявления опухоль чаще всего достигает значительных размеров, прорастая в рядом расположенные сосуды, и радикальная операция становится невозможна. Исходя из этого, предлагают следующие критерии, наличие которых допускает возможность резектабельности: отсутствие метастазов; отсутствие или небольшое вовлечение в опухолевый процесс крупных сосудов; при вовлечении вен должна иметься возможность их реконструкции; пациент должен быть в состоянии перенести оперативное вмешательство. При поражении головки поджелудочной железы производят процедуру Whipple — панкреатодуоденэктомию. В случае поражения тела и хвоста проводят дистальную панкреатэктомию.
Химиотерапия проводится в двух вариантах: адъювантном и неоадъювантном. Неоадъювантная терапия позволяет уменьшить размеры опухоли, более четко разграничить здоровые и пораженные ткани, для того чтобы хирургическая операция имела больше шансов на успех. Адъювантная химиотерапия, согласно рекомендациям Национальной всеобщей онкологической сети, рекомендована пациентам, хорошо перенесшим резекцию. При нерезектабельной опухоли и отдаленных метастазах проводят паллиативную химиотерапию. Лучевая терапия — довольно неоднозначный метод лечения. Существуют различные данные об ее эффективности. В некоторых случаях вред, причиняемый здоровым тканям поджелудочной железы и окружающим органам превышает и без того незначительную эффективность. Однако иногда неоадъювантная лучевая терапия достаточно успешно уменьшает размеры опухоли, обеспечивая ее резектабельность.
Возлагаются большие надежды на таргетную и иммунную терапию. Активно изучаются методы воздействия на онкоген K-ras. Таргетное уменьшение размеров стромы снизит злокачественность и позволит с большей эффективностью проводить лечение аденокарциномы поджелудочной железы.
Разрабатываются вакцины, эффективность которых уже начали испытывать. Прогноз при протоковой аденокарциноме поджелудочной железы неблагоприятный. Пятилетняя выживаемость достигает 7,2%. У прооперированных пациентов она может возрастать до 22%.
Devita Jr V. T., Lawrence T., Rosenberg S. A. Cancer: Principles & Practice of Oncology: Annual Advances in Oncology. – Lippincott Williams & Wilkins, 2012.
Pancreatic Ductal Adenocarcinoma [Электронный ресурс]. – Режим доступа: https://www.pancreapedia.org/reviews/pancreatic-ductal-adenocarcinoma, свободный. – Загл. с экрана.
Pancreatic Cancer Treatment (PDQ®)–Patient Version [Электронный ресурс]. – Режим доступа: https://www.cancer.gov/types/pancreatic/patient/pancreatic-treatment-pdq#section/_162, свободный. – Загл. с экрана.
Stark A. P. et al. Long-term survival in patients with pancreatic ductal adenocarcinoma //Surgery. – 2016. – Т. 159. – №. 6. – С. 1520-1527.
Впервые опухоль описана в 1982 г. как новообразование с гиперпродукцией муцина, располагающееся внутри протоков ПЖ с экзофитным ростом в виде сосочков (триада К. Охеши). В течение последующего десятилетия появлялись единичные сообщения о выявлении муцинозных злокачественных опухолей ПЖ, однако отсутствие единого определения не позволяло классифицировать эти находки. Только в 1994 г. для таких опухолей было предложено вышеуказанное название, которое вошло в общепринятую терминологию и сохранилось и по сей день. С тех пор число публикаций, посвященных этой проблеме, резко увеличилось.
Эпидемиология
Внутрипротоковые папиллярные муцинозные опухоли относительно редки, их доля составляет до 3% от всех экзокринных опухолей ПЖ и 18% среди кистозных опухолей ПЖ. Несколько чаще болеют мужчины; возрастной диапазон при первичной диагностике составляет 37—80 лет (чаще 60—70 лет), средний возраст — 64 года. Вероятно, истинная частота внутрипротоковых папиллярных муцинозных опухолей значительно выше, поскольку многим больным выставляют диагноз острого или хронического панкреатита, что обусловлено рядом причин.
Во-первых, средний возраст клинической манифестации этой опухоли составляет 60-70 лет, когда подавляющее большинство больных имеет тяжелые сопутствующие заболевания, каждое из которых может привести к смерти. Во-вторых, аутопсию проводят не у всех больных, а если и выполняют, то при очевидной причине смерти (например, при остром инфаркте миокарда), поэтому ПЖ не уделяют должного внимания. По нашему опыту работы с различными отечественными патоморфологами при отсутствии макроскопически или пальпаторно определяемой опухоли, вскрытие ПЖ по её протоку практически не проводят.
Поскольку опухоль папиллярная, пропальпировать её невозможно, в ряде случаев невозможно даже увидеть её при осмотре макропрепарата (на поперечном срезе протока). Только лишь в том случае, если больной скончался от диагностированного обструктивного панкреатита, причина которого не ясна, есть хороший шанс диагностировать эту опухоль на аутопсии. В-третьих, внутрипротоковая папиллярная опухоль склонна к медленному прогрессированию. Аналогично (с длительно сохраняющимися симптомами) протекает и ХП.
При адекватной лекарственной терапии и отсутствии серьёзного мониторинга (с использованием всех доступных методик визуализации) как исходно, так и в динамике, течение заболевания может продолжаться несколько лет, пока не произойдёт озлокачеетвление со всеми вытекающими последствиями. В-четвёртых, как ни печально это признавать, значительный вктад в гиподиагностику внутрипротоковых папиллярных муцинозных опухолей вносит низкая осведомлённость как практических врачей, так и некоторых морфологов о существовании этой опухоли.
Патоморфология
Опухоль характеризуется внутрипротоковой пролиферацией муцинпродуцирующих клеток, располагающихся в виде сосочков. Гиперсекреция муцина и затруднение оттока секрета при большом количестве сосочков в пределах одного протока может приводить к его кистозному расширению. Если очагов опухолевого роста несколько (фокальный или диффузный тип опухоли), расширение протоков ПЖ выше места сужения может носить ограниченный характер.
Клеточная атипия варьирует от минимальной до тяжёлой, что предполагает подразделение этих опухолей на аденомы, пограничные опухоли и интрацуктальные карциномы (т.е. на доброкачественные, пограничные и злокачественные опухоли). Кроме того, кпеточная дифференцировка может быть различной — интестинальной, панкреатобилиарной и онкокистозной. В основном внутрипротоковые папиллярные муцинозные опухоли растут медленно, однако в 30% случаев они прорастают окружающие ткани и метастазируют. Наиболее частое расположение опухоли — проток ПЖ в проекции её головки. Предполагают, что опухоли, возникшие из второстепенных протоков, имеют лучший прогноз, нежели те, что происходят из основного протока ПЖ.
До сих пор отсутствуют иммуногистохимические и молекулярные маркёры опухоли, не совсем изучены механизмы изменчивости папиллярного компонента, степени секреции муцина, причин вариабельного распространения опухоли и т.п. В ряде случаев эту опухоль крайне трудно отличить от других новообразований, в частности от панкреатической интраэпителиальной неоплазии (PanlNs), поэтому в последние годы в действующую классификацию внесены поправки, благодаря которым можно разграничить эти опухоли.
Этиопатогенез
Этиопагогенез внутрипротоковых папиллярных муцинозных опухолей в настоящее время остаётся загадкой. Интересен следующий факт — такая опухоль, ассоциированная с цистадеиокарциномой, гистологически характеризуется наличием инвазивного компонента с трубчатой или муцинозной структурой. Тубулярная инвазия имеет сходство с протоковой цистадеиокарциномой, в то время как муцинозная часть опухоли представлена коллоидом (муцинозная некистозная карцинома). Кроме того, внутрипротоковые папиллярные опухоли с тубулярной, подобной протоковой иистаденокарциноме, инвазией, характеризуются панкреатобилиарным типом дифференцировки клеток, в то время как опухоль с муцинозноподобной инвазией характеризуется гастроинтестинальным фенотипом.
Исследования последних лет, в некоторой степени приоткрывающие завесу таинственности над патогенезом этой опухоли, посвящены изучению продукции муцина опухолевыми клетками. Было обнаружено, что опухоли с различной дифференцировкой клеток (разным фенотипом) продуцируют разные муцины. Так, опухоли с гастроинтестинальным фенотипом, продуцируют MUC-2, а опухоли с панкреатобилиарным фенотипом — только MUC-1. Кроме того, был обнаружен третий тип опухоли, способный к одновременной продукции муцинов обоих типов — MUC-1 и MUC-2.
Эта разновидность в последствии была названа онкокистозным подтипом внутрипротоковой папиллярной муцинозной опухоли. Результаты этих исследований наводят на мысль, что термин внутрипротоковая папиллярная муцинозная опухоль — собирательное понятие, объединяющее, по крайней мере, три разновидности опухолей, достаточно близких по строению, но различных по иммунофенотипу секретируемого ими муцина. Наиболее часто выявляют гастроинтестинальный MUC-2- фенотип.
Гастроинтестинальный MUC-2+ фенотип составляет одну иммунофенотипическую группу с MUC-2+ коллоидной (муцинозной некистозной) карциномой, что предполагает возможность превращения внутрипротоковой папиллярной муцинозной опухоли в эту разновидность злокачественного новообразования. MUC-l+ панкреатобилиарный тип связан, возможно, с протоковой цистадеиокарциномой. Третий тип протоковой папиллярной опухоли — онкокистозный, возможно, может озлокачествляться, трансформируясь в карциному, однако гистологические и биологические особенности последней остаются неизученными.
Молекулярные механизмы, вктючающиеся при нарушении регуляции гена MUC при внутрипротоковой папиллярной опухоли, остаются пока неизвестными. Возможно, они определяются другими клетками, что косвенно подтверждается различным прогнозом при разных типах папиллярной опухоли — как мы отмечали выше, MUC-2+ тип отличается более благоприятным течением. Существует предположение о существовании неидентифицированной в настоящее время мутации, определяющей развитие интрадуктальной папиллярной муцинозной опухоли. Предположение это основано на факте частой ассоциации этих опухолей с другими внепанкреатическими злокачественными новообразованиями, а также с синдромом Пейтца—Егерса. Диагностика
Клиническая картина
Характерны симптомы острого или хронического панкреатита, реже опухоль выявляют случайно. Частота тяжёлых деструктивных панкреатитов при внутрипротоковой папиллярной опухоли не превышает 2%.
Большинство симптомов аналогичны таковым при ХП — боли в эпигастрии с усилением после приёма пищи, диспептические расстройства, астенические симптомы, признаки эндо- и экзокринной недостаточности, похудание.
Механическая желтуха возникает в 20% случаев, сс появление косвенно свидетельствует о злокачественном варианте опухоли. Крайне редко обнаруживают асцит.
Частота встречаемости сахарного диабета при внутрипротоковых папиллярных муцинозных опухолях достигает 11%, однако истинная причина эндокринной недостаточности до сих пор не установлена. Если речь идёт о протоковой аденокарциноме, быстро распространяющейся по паренхиме ПЖ с замещением опухолевой тканью островков Лангерганса, то, как правило, говорят о панкреатогенном сахарном диабете, вторичном по отношению к раку ПЖ. При внутрипротоковых папиллярных опухолях инвазия в паренхиму ПЖ происходит не так часто, и менее выражена, чем при раке, поэтому механизм диабета при этих новообразованиях не совсем понятен. Возможно, сахарный диабет развивается на фоне рецидивирующего обструктивного панкреатита, приводящего к воспалительным, деструктивным, кистозным, фиброзным и атрофическим изменениям как экзо-, так и эндокринной части ПЖ.
Дефицит массы тела обнаруживают у 42% больных. Как и при панкреатите, он обусловлен рядом причин. Во-первых, гиперпродукция муцина на ранних этапах развития опухоли может приводить с временной обструкции выводных протоков ПЖ, что обусловливает болевой абдоминальный синдром после приёма пищи. Дальнейший рост опухоли приводит к уменьшению просвета поражённого протока (или протоков) с нарастанием клинических проявлений. Боль вынуждает больных отказываться от приёма пищи, чтобы предотвратить, таким образом, её повторное возникновение (ситофобия). Во-вторых, растущая, метаболически активная опухоль потребляет для собственных нужд всё необходимое. Нарушение обмена веществ обусловлено и сахарным диабетом, осложняющим течение опухоли.
В-третьих, нарушенный отток панкреатического сока в просвет ДПК приводит к развитию экзокринной недостаточности ПЖ, способствуя нарушению пищеварения и всасывания питательных веществ.
Методы визуализации. Для скрининга, как и при других опухолях ПЖ, используют УЗИ и КТ. Эффективность диагностики существенно повышается при информированности врачей о существовании этой необычной опухоли. На эффективность диагностики влияет также расположение опухоли (в основном протоке ПЖ или в более мелких протоках).
Во всех случаях, когда при скрининговом УЗИ выявляют дилатацию протока ПЖ при отсутствии объективной причины блока (опухоли головки ПЖ больших размеров, камней в общем жёлчном протоке, опухоли БДС и т.п.) и анамнестических данных заранее имевшую место патологию, способствующую развитию Рубцовых изменений БДС и терминального отдела протока ПЖ, в первую очередь надо думать о наличии у больного внутрипротоковой папиллярной опухоли. При диффузной форме опухоли может быть расширено несколько протоков, при сегментарной — как правило, один.
Другой важнейший признак внутрипротоковых папиллярных опухолей — распространённая атрофия паренхимы ПЖ, обычно пропорциональная степени протоковой дилатации. Далеко не всегда при УЗИ можно выявить чёткие зоны внутрипротоковых блоков, а уж тем более определить, чем они вызваны — муциновыми «пробками» или папиллярными разрастаниями. Третий признак опухоли патогномоничен — наличие гипоэхогенных микро- или макрокистозных изменений паренхимы ПЖ по типу «пчелиных сот»; связь этих кист с дилатированными протоками при УЗИ выявляют не всегда.
В ряде случаев у больных обнаруживают кальцификацию и панкреатолитиаз, обусловленные как рецидивирующим панкреатитом, так и отложением солей кальция в муциновых «пробках».
При КТ с контрастированием зона опухоли значительно лучше накапливает контрастное вещество, чем окружающая паренхима. В просвете расширенного протока ПЖ можно выявить гиперэхогенные включения, соответствующие муциновым «пробкам» или папиллярным разрастаниям.
При длительном течении новообразования, расположенного в головке ПЖ, опухолевая инфильтрация вместе с кистозными изменениями протоков может достигать больших размеров, занимая всю головку железы. В результате сдавливается интрапанкреатический отдел общего жёлчного протока с развитием билиарной гипертензии. В ряде случаев у больных возникает асцит, обусловленный пропотеванием жидкостного компонента кист, поскольку стенка кист может быть достаточно тонкой, а давление внутри кист значительно большим, чем в полости брюшины.
Выраженная протоковая дилатация при отсутствии атрофических изменений паренхимы, особенно при наличии чётко определяемых внутрилротоковых папиллярных разрастаний, — признак озлокачествления опухоли. Даже при начальных этапах озлокачесгвления всегда присутствует кистозный компонент, что важно учитывать при дифференциальной диагностике с протоковой аденокарциномой. Наличие кистозного расширения коллатеральных протоков в сочетании с внутрипротоковыми разрастаниями существенно упрощает диагностику диффузных форм. При сегментных формах результаты КТ не столь специфичны.
Несмотря на ряд условно специфичных признаков при УЗИ, КТ и МРТ, необходимо выявить сами внутрипротоковые папиллярные разрастания. Ранее с этой целью применяли только ЭРХПГ, однако совершенствование программ КТ и МРТ, появление ЭУС и МРХПГ позволяет в настоящее время с достаточной точностью выявлять внутрипротоковые разрастания. Достаточно чувствительный метод диагностики внутрипротоковых папиллярных опухолей — проведение МРХПГ с внутривенным ведением карбахола (секретина). Самый современный метод диагностики, позволяющий осуществить визуальный осмотр протока ПЖ и произвести биопсию опухоли. — вирсунгоскопия, дополняющая ЭУС.
Дифференциальная диагностика с первичными панкреатитами основана на возрастном критерии (в среднем 42 года при рецидивируюшем хроническом панкреатите), половом критерии (хроническим панкреатитом, не связанным с очевидной патологией билиарного тракта, страдают преимущественно мужчины), а также на факте отсутствия у многих больных внутрипротоковой папиллярной опухолью отягощенного анамнеза по злоупотреблению алкоголем и табакокурению.
Дифференциальная диагностика с серозной цистаденомой достаточно трудна и основана на возрастных (при пистаденомах средний возраст больных на Шлет меньше), половых (цистаденома встречается у женщин в 7 раз чаще) отличиях и более благоприятном течении (чаше скрытом) цистаденомы. Расположение опухоли, демографические признаки, образ жизни не позволяют разграничить эти кистомы. Внутрипротоковая папиллярная опухоль чаще протекает с клиническими проявлениями и с развитием осложнений, чем при цистаденомах.
Дифференциальная диагностика с муцинозной цистаденомой также трудна, однако она имеет меньшее значение, поскольку в обоих случаях показано радикальное хирургическое лечение. Отмечают некоторые возрастно-половые, клинические и топографические отличия, поскольку мупинозная цистаденома встречается, в подавляющем большинстве случаев, у женщин среднего возраста, в 93% случаев она располагается в теле и хвосте ПЖ, практически всегда протекает бессимптомно.
Лечение
Всем больным внутрипротоковой папиллярной муцинозной опухолью показано хирургическое лечение в виде панкреатодуоденальной резекции либо панкреатэктомии, несмотря на высокий средний возраст больных (65—70 лет), имеющих много сопутствующих заболеваний. До операции должен быть установлен морфологический диагноз.
Ориентация на хирургическое лечение у всех больных в обязательном порядке вполне оправдана, поскольку даже при доброкачественной папиллярной опухоли на момент первичного установления диагноза риск озлокачествления высок; значительна вероятность развития рецидивирующего обструктивного панкреатита, грозного своими осложнениями. В специализированных центрах, занимающихся хирургией ПЖ, летальность после панкреатодуоденальной резекции при внутрипротоковых папиллярных муцинозных опухолях не превышает 5%, при дистальной резекции смертельных случаев, как правило, и вовсе нет.
Источник статьи: http://mr-gergebil.ru/intrajepitelialnaja-neoplazija-podzheludochnoj-zhelezy/