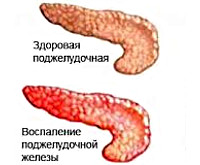
Этиология и патогенез при заболеваниях поджелудочной железы
Патогенез острого панкреатита достаточно исследованная проблема, которая имеет важное значение в изучении заболеваний желудочно-кишечного тракта.
Панкреатит, вопреки расхожему мнению, это не одно конкретное заболевание, а целая группа синдромов и патологических состояний, которые характеризуются воспалением поджелудочной железы. Кроме прочего, данное состояние характеризуется наличием дегенеративных процессов, то есть изменений тканей поджелудочной железы. Острый панкреатит, в свою очередь, это остро протекающее воспалительное заболевание, имеющее полиэтиологическую природу. Для того чтобы понять суть возникающих патологических процессов, следует знать о некоторых особенностях анатомии и физиологии поджелудочной железы.
Поджелудочная железа – часть пищеварительной системы человека. Это достаточно крупная железа, которая одновременно является железой внешней и внутренней секреции. С одной стороны, поджелудочная железа выделяет специфические ферменты, участвующие в процессе пищеварения, а с другой, производит гормоны, принимающие активное участие в обмене белков, жиров и углеводов. Таким образом, любые функциональные нарушения в работе поджелудочной железы приводят к серьезным проблемам в организме в целом. Секреты поджелудочной железы нейтрализуют кислую среду желудка, а потому нарушения в работе этой железы приводят, кроме прочего, к повышению кислотности и к проблемам связанным с этим.
Анатомия поджелудочной железы

Формирование поджелудочной железы начинается еще в эмбриональном периоде (примерно 3 неделя беременности) и полностью заканчивается у детей 5-6 года жизни. У новорожденных поджелудочная железа имеет малый размер и достаточно подвижна.
Этиология острого панкреатита
Острый панкреатит является одним из трех заболеваний ЖКТ, которые наиболее распространены в практика врачей-гастроэнтерологов и требуют лечения в стационаре. Количество людей, страдающих данным заболеванием, ежегодно растет, а их возраст становится все более юным. По мнению специалистов, причина такого положения кроется в том, что молодые люди все реже придерживаются принципов здорового образа жизни и диетического питания. Среди наиболее распространенных причин возникновения острого панкреатита у пациентов среднего возраста отмечается злоупотребление алкоголем и вредные пищевые привычки. Острая, соленая и другая “агрессивная” пища, которая употребляется с завидной регулярностью, может стать причиной развития заболевания или рецидива уже имеющейся патологии.

- наличие в анамнезе желчнокаменной болезни;
- бактериальное поражение органов желудочно-кишечного тракта;
- различные общие инфекционные заболевания;
- травмы железы;
- хирургические вмешательства по поводу различных патологических состояний желчевыводящих путей;
- воспалительные заболевания органов пищеварения;
- системный и длительный прием некоторых лекарственных препаратов (диуретиков, кортикостероидов, азатиоприна и т.д.);
- врожденные или приобретенные аномалии развития железы;
- тяжелые аутоиммунные заболевания (муковисцидоз и другие);
- генетическая предрасположенность пациента и т.д.
Патогенез острого панкреатита
Патогенез острого панкреатита – это достаточно сложная цепь изменений, которые затрагивают не только поджелудочную железу, но и весь организм в целом. Какие механизмы начинают работать при наличии вышеупомянутых факторов и почему возникает данное патологическое состояние? Прежде всего, стоит отметить, что любая из причин развития панкреатита провоцирует нарушение тока панкреатического сока и активное образование ферментов данной железы. То есть возникает следующая ситуация: поджелудочная железа активно вырабатывает ферменты, но их естественный ток нарушен.

- спазм сфинктера поджелудочной железы;
- рефлюкс (неправильное или ретроградное движение) дуоденального содержимого;
- отек сосочков;
- рефлюкс желчи;
- активация образования ферментов и т.д.
Нарушенный, по вышеуказанным причинам, отток секреторного содержимого поджелудочной железы приводит к тому, что возникает повышенное гидростатическое давление в протоках поджелудочной железы. Именно гипертензия (повышенное давление) разрушающе действует на клетки поджелудочной железы, что и приводит к возникновению острого воспалительного процесса. Патогенез острого панкреатита сопровождается сильным отеком тканей, а также поражением сосудов железы.
Кроме прочего, ферментное содержимое воспаленной поджелудочной железы имеет свойство попадать в общий кровоток. Именно это становится причиной ряда общих нарушений состояния пациента. Попадая в кровь, ферменты поджелудочной железы повреждают глобулины и различные белки сыворотки крови. При этом образуется большое количество продуктов распада, которые разносятся кровотоком во все органы и системы человека, что приводит к нарушению их функций и даже разрушению. Именно в связи с тем, что в кровь попадают продукты распада, у пациентов, страдающих данным заболеванием, часто наблюдаются признаки общей интоксикации организма (повышение температуры тела, тошнота и рвота, нарушение общего соматического состояния и другие). Также интоксикация нередко становится причиной состояний, угрожающих не только здоровью, но и жизни пациента.
Как проявляется острый панкреатит?

Болевой синдром может локализоваться в области эпигастрия, иметь опоясывающий характер, отдавать в левое подреберье или постоянно быть в этой области. Кроме сильной боли, характерными диагностическими признаками острого панкреатита являются:
- тошнота;
- неукротимая рвота, не приносящая пациенту должного облегчения;
- резкое повышение температуры тела до фебрильных показателей;
- желтушность кожных покровов различной интенсивности.
У некоторых пациентов наблюдаются кровоизлияния в области пупочного кольца, а также вздутие живота, изжога и другие клинические симптомы. В клиническом течении заболевания отмечается некоторая цикличность. В первые сутки у пациентов наблюдается сильный болевой синдром, что является основным диагностическим признаком. На вторые сутки боль становится менее интенсивной, но нарастают явления общей интоксикации. На 5-6 сутки наступает улучшение, но опасность составляют вторичные поражения и гнойные осложнения заболевания.
Следует заметить, что острый панкреатит – это серьезное заболевание, которое при отсутствии адекватной терапии может привести к летальному исходу или возникновению серьезных осложнений. Наличие симптомов острого панкреатита должно стать для пациента поводом немедленно вызвать скорую помощь. Данное заболевание в большинстве случаев подлежит лечению в условиях специализированного стационара, а в особо тяжелых клинических случаях требует хирургического вмешательства.
Не стоит забывать, что именно несвоевременное обращение к врачам часто становится причиной непоправимых последствий.
Панкреатит
представляет собой тяжелое заболевание
поджелудочной железы, в основе которого
лежит внутриорганная активация
продуцируемых железой пищеварительных
ферментов и выраженное в различной
степени ферментативное повреждение
ткани (панкреонекроз), с последующим
развитием фиброза, нередко распространяющееся
на окружающие ткани (парапанкреофиброз),
а также осложняемое вторичной инфекцией.
Клинически панкреатит может протекать
в острой и хронической формах, нередко
тесно связанных между собой.
Этиологией
возникновения хронического панкреатита
являются:
1.
Алкоголь, раздражая слизистую оболочку
12 п.к„ не только усиливает продукцию
секретина, панкреозимина, гистамина,
гастрина, а, следовательно, и внешнюю
секрецию ПЖ, но и вызывает рефлекторный
спазм сфинктера Одди, приводящий к
внутрипротоковой гипертензии. Длительное
употребление алкоголя сопровождается
дуоденитом с нарастающей атонией
сфинктера, что приводит к
дуоденопанкреатическому и
билиарнопанкреатическому рефлюксу,
особенно во время рвоты. Имеет значение
и белково-витаминная недостаточность
свойственная хроническому алкоголизму.
Некоторые авторы полагают, что алкоголь
может оказывать и прямое токсическое
воздействие на паренхиму ПЖ. Кроме того,
имеются данные, что хроническая
алкогольная интоксикация изменяет
состав панкреатического сока за счет
увеличения количества белка, лактоферрина
и снижения бикарбонатов и ингибиторов
протеаз, что способствует образованию
конкрементов.
2.
Заболевания желчного пузыря и
желчевыводящих путей, при доминировании
желчнокаменной болезни, включая и
состояние после холецистэктомии.
Сопровождающий эти заболевания
воспалительно-склеротический процесс
в дистальных отделах желчевыводящих
путей приводит к стенозу, либо
недостаточности сфинктера Одди. Спазм
или стеноз сфинктера приводят к
гипертензии в протоковой системе ПЖ и,
как следствие, выходу компонентов
панкреатического сока в паренхиму с
развитием в ней воспалительных и
склеротических изменений. Рефлюкс желчи
при этом не имеет решающего значения,
так как ХП развивается и при раздельном
впадении холедоха и вирсунгиева протока
в 12 п.к. Слизистая оболочка панкреатических
протоков в норме резистентна к действию
желчи, и только при длительной инкубации
желчи в смеси с панкреатическим секретом
или культурой бактерий желчь приобретает
повреждающее действие на ПЖ. В случае
недостаточности большого дуоденального
соска происходит рефлюкс кишечного
содержимого в протоки ПЖ с активацией
протеолитических ферментов, что в
сочетании с гипертензией и оказывает
повреждающее воздействие на паренхиму
органа.
3. Травма ПЖ, в том
числе интраоперационная, В развитии
послеоперационного панкреатита имеет
значение не только прямое воздействие
на ткань железы и ее протоки, но и
деваскуляризация ПЖ,
4.
Заболевания желудочно-кишечного тракта,
особенно 12 п.к.: отек в области Фатерова
соска, затрудняющий отток панкреатического
секрета, дуоденостаз, сопровождающийся
дуоденопанкреатическим рефлюксом;
дивертикулы 12 п.к., которые могут
приводить либо к сдавлению протоков с
последующей гипертензией, либо, в
случае открытия протока в дивертикул-
к дуоденопанкреатическому рефлюксу.
Дуоденит не только поддерживает
воспаление Фатерова соска, но и вызывает
секреторную дисфункцию ПЖ вследствие
нарушения продукции полипептидных
гормонов ЖКТ. Пенетрация язвы 12 п.к.
или желудка в ПЖ чаще приводит к очаговому
воспалительному процессу, а в ряде
случаев — к типичному хроническому
рецидивирующему панкреатиту.
5.
Одностороннее питание углеводной и
жирной пищей при недостатке белков
ведет к резкой стимуляции внешней
секреции с последующим срывом
регенераторных процессов в ПЖ.
Особенно большое значение имеет прием
алкоголя с жирной пищей.
6.
Эндокринопатии и нарушения обмена
веществ:
—
гиперпаратиреоз, который ведет к
гиперкальцисмии и кальцификации ПЖ
/кальций способствует переходу
трипсиногена в трипсин в протоках ПЖ
—
гиперлипидемия, которая ведет к жировой
инфильтрации клеток ПЖ, повреждению
сосудистой стенки, образованию тромбов,
микроэмболии сосудов;
7.
Аллергические факторы. В крови ряда
больных обнаруживаются антитела к ПЖ;
в некоторых случаях отмечается выраженная
эозинофилия (до 30-40% и более). В литературе
описаны случаи появления болевых кризов
при употреблении клубники, и развития
ХП на фоне бронхиальной астмы.
8.
Наследственные факторы. Так известно,
что у детей, родители которых страдают
ХП, повышена вероятность его развития
по аутосомно-доминантному типу.
Подчеркивается более частая встречаемость
ХП у лиц с 0(1) группой крови. В некоторых
случаях это бывает причиной так называемых
ювенильных панкреатитов.
9.
Пороки развития панкреобилиодуоденапьной
зоны: кольцевидная ПЖ, сопровождающаяся
дуоденостазом; добавочная ПЖ с различными
вариантами хода протоков, не обеспечивающими
отток секрета; энтерогенные кисты ПЖ.
10.
Лекарственные препараты: стероидные
гормоны, эстрогены, сульфаниламиды,
метилдофа, тетрациклин, сульфасалазин,
метронидазол, ряд нестероидных
противовоспалительных средств,
иммунодепрессанты, антикоагулянты,
ингибиторы холинэстеразы и другие.
11.
Неспецифический язвенный колит, болезнь
Крона, гемохроматоэ и ряд других
заболеваний, сопровождающихся
склеротическими изменениями в ПЖ без
клинической манифестации, что можно
рассматривать как неспецифическую
тканевую реакцию на токсические или
циркуляторные воздействия. В эту же
группу, вероятно, следует отнести фиброз
ПЖ при циррозах печени.
12.
Инфекционные и паразитарные болезни:
эпидемический паротит, вирусный гепатит,
инфекционный мононуклеоз, брюшной тиф,
туберкулез, сифилис, кишечные инфекции,
амебиаз и т.д., сопровождающиеся межуточным
воспалением ПЖ с последующим ее склерозом.
Патогенез.
Можно считать общепризнанным, что в
основе патогенеза панкреатита у
подавляющего большинства больных лежит
повреждение ткани железы ею же
продуцируемыми пищеварительными
ферментами. В норме эти ферменты
выделяются в неактивном состоянии
(кроме амилазы и некоторых фракций
липазы) и становятся активными лишь
после попадания в двенадцатиперстную
кишку. Большинство современных авторов
выделяют три главных патогенетических
фактора, способствующих аутоагрессии
ферментов в секретирующем их органе:
1)
затруднение оттока секрета железы в
двенадцатиперстную кишку и внутрипротоковая
гипертензия;
2)
ненормально высокие объем и ферментативная
активность сока поджелудочной железы;
3) рефлюкс в
протоковую систему поджелудочной железы
содержимого двенадцатиперстной кишки
и желчи.
Механизмы
патологической внутриорганной активации
ферментов и повреждения ткани железы
различаются в зависимости от причины
панкреатита. Так известно, что алкоголь,
особенно в больших дозах, рефлекторным
и гуморальным путем резко повышает
объем и активность панкреатического
сока. К этому дбавляется стимулирующее
действие алиментарного фактора, поскольку
алкоголики питаются нерегулярно, не
столько едят, сколько закусывают,
принимая много жирной и острой пищи.
Кроме того, алкоголь способствует спазму
сфинктера печеночно-панкреатической
ампулы (сфинктера Одди), вызывает
повышение вязкости панкреатического
секрета, образование в нем белковых
преципитатов, в дальнейшем трансформирующихся
в конкременты, характерные для хронической
формы заболевания. Все это затрудняет
отток секрета и ведет к внутрипротоковой
гипертензии, которая при уровне,
превышающем 35-40 см вод. ст., способна
обусловить повреждение клеток эпителия
протоков и ацинусов и освобождение
цитокиназ, запускающих механизм активации
ферментов. Спазм сфинктера Одди, возможно,
ведет к желчно-панкреатическому рефлюксу
и внутрипротоковой активации ферментов
за счет желчных кислот. Не исключают
также и прямое повреждающее действие
высоких концентраций алкоголя в крови
на железистые клетки.
При
панкреатите, связанном с заболеваниями
желчных путей, главным патогенетическим
фактором является нарушение оттока
панкреатического сока в двенадцатиперстную
кишку, что связано, прежде всего, с
наличием упоминавшегося «общего канала»,
то есть печеночно-панкреатической
(фатеровой) ампулы, через которую отходят
желчные конкременты и куда обычно
впадает главный панкреатический проток.
Известно, что при раздельном впадении
желчного и панкреатических протоков,
а также при отдельном впадении в
двенадцатиперстную кишку добавочного
протока, сообщающегося с главным протоком
поджелудочной железы, билиарный
панкреатит не развивается.
Проходя
через фатерову ампулу, желчные конкременты
временно задерживаются в ней, вызывая
спазм сфинктера Одди и преходящую
протоковую гипертензию, обусловливающую
ферментативное повреждение ткани железы
и, возможно, приступ острого панкреатита,
в ряде случаев протекающий малосимптомно
или же маскирующийся приступом желчной
колики. Повторное «проталкивание»
желчных камней через ампулу за счет
высокого панкреатического и билиарного
давления может привести к травме
слизистой дуоденального сосочка и
стенозирующему панпиллиту, все более
затрудняющему пассаж желчи и
панкреатического сока, а также и повторное
отхождение камней. Иногда наступает
стойкое ущемление желчного конкремента
в ампуле, ведущее к обтурациониой желтухе
и тяжелому панкреонекрозу.
Самостоятельную
роль в патогенезе панкреатита могут
играть также заболевания двенадцатиперстной
кишки, связанные с дуоденостазом и
гипертензией в ее просвете и способствующие
рефлюксу дуоденального содержимого в
панкреатический проток (в том числе
«синдром приводящей петли» после
резекции желудка по типу Бильрот П).
Некоторые авторы указывают и на значение
дивертикулов двенадцатиперстной кишки,
в особенности перипапиллярных, которые
могут обусловливать как спазм, так и
(редко) атонию сфинктера Одди.
Травматический
панкреатит может быть связан как с
прямым, так и с опосредованным воздействием
на поджелудочную железу. При прямой
травме к внутриорганной активации
ферментов ведет механическое повреждение
железы с выделением из омертвевающих
клеток уже упоминавшихся активаторов
(цитокиназ) и последующим развитием в
дополнение к травматическому еще и
ферментативного панкреонекроза. При
эндоскопических вмешательствах на
большом дуоденальном сосочке (РХПГ,
ЭПСТ) часто травмируется слизистая
оболочка фатеровой ампулы и терминального
отдела главного панкреатического
протока. В результате травмы кровоизлияний
и реактивного отека может затрудняться
отток панкреатического секрета и
развиваться протоковая гипертензия.Стенки
протока могут повреждаться и от
избыточного давления при введении
контрастного вещества при РХПГ.
При
опосредованном воздействии случайных
и операционных травм на поджелудочную
железу (травматический шок, кровопотеря,
кардиохирургические вмешательства с
длительной перфузией) повреждение
железистой ткани с высвобождением
активирующих клеточных факторов связано
в основном с микроциркуляторными
расстройствами и соответствующей
гипоксией.
Следует
обратить внимание на еще один важный
аспект патогенеза хронического
панкреатита, недостаточно освещаемый
в литературе. По представлениям
большинства клиницистов панкреонекроз
считается определяющей особенностью
наиболее тяжелых форм острого
деструктивного панкреатита. Однако
повреждение и гибель (омертвение, некроз)
ткани поджелудочной железы под
воздействием внутриорганной активации
и аутоагрессии пищеварительных ферментов
определяет возникновение и течение
любых, в том числе и хронических, форм
рассматриваемого заболевания.
При
хроническом панкреатите, не являющемся
следствием острого, также имеет место
ферментативное повреждение, некробиоз,
некроз и аутолиз панкреатоцитов,
происходящие как постепенно, под влиянием
длительно действующего фактора, так и
остро скачкообразно в период обострений
хронического процесса.
Патологическая
анатомия.
В процессе развития панкреатита в ткани
поджелудочной железы происходит
разрастание соединительной ткани, в
результате чего развивается фиброз и
склероз. В дальнейшем развиваются
обызвествление, нарушение проходимости
панкреатических протоков..
Источник статьи: http://mr-gergebil.ru/jetiologija-i-patogenez-pri-zabolevanijah-podzheludochnoj-zhelezy/
ПАНКРЕАТИТ
ПАНКРЕАТИТ (pancreatitis; греч, pankreas, pankreatos поджелудочная железа + -itis) — воспаление поджелудочной железы.
В клинической практике встречаются две основные формы заболевания — острый и хронический Панкреатит.
Содержание
- 1 Острый панкреатит
- 1.1 Классификация
- 1.2 История
- 1.3 Статистика
- 1.4 Этиология
- 1.5 Патогенез
- 1.6 Патологическая анатомия
- 1.7 Клиническая картина
- 1.8 Осложнения
- 1.9 Диагноз
- 1.10 Лечение
- 1.11 Прогноз и Профилактика
- 1.12 Особенности острого панкреатита у детей
- 2 Хронический панкреатит
- 2.1 Этиология и патогенез
- 2.2 Патологическая анатомия
- 2.3 Клиническая картина
- 2.4 Диагноз
- 2.5 Лечение
- 2.6 Особенности хронического панкреатита в пожилом и старческом возрасте
- 3 Экспериментальный панкреатит
- 4 Таблица. Дифференциально-диагностические признаки основных форм острого панкреатита
Острый панкреатит
Острый П.— воспалительно-некротическое поражение поджелудочной железы, развивающееся в результате ферментативного аутолиза, или самопереваривания.
Классификация
Предложено св. 40 классификаций острого П. V Всероссийский съезд хирургов в 1978 г. рекомендовал пользоваться следующей классификацией острого П.: 1) отечный П.; 2) жировой панкреонек-роз; 3) геморрагический панкреонек-роз; 4) гнойный П. Эта классификация, основанная на морфол, принципе, не отражает другие аспекты заболевания, имеющие важное значение для леч. тактики. Для более точной оценки клин, течения необходимо выделить три фазы заболевания: 1) фаза энзимной токсемии; 2) фаза времен-, ной ремиссии; 3) фаза секвестрации и гнойных осложнений.
При осложненном течении П. необходимо оценить распространенность перитонита и характер выпота в брюшинной полости. При распространении процесса на забрюшинную клетчатку следует выяснить степень поражения ее. Кроме того, нужно учитывать степень поражения ткани поджелудочной железы, к-рое может носить ограниченный, субтотальный или тотальный характер. При жировом панкреонекрозе очаги некроза на поверхности железы могут иметь очаговый или сливной характер.
История
В 1841 г. Тульп (N. Tulp) сообщил об абсцессе поджелудочной железы, обнаруженном при вскрытии больного, умершего при симптомах острого живота. Клебс (E. Klebs) в 1870 г. выделил острый П. как отдельное заболевание. Фитц (R. H. Fitz) в 1889 г. сделал сообщение о том, что он распознал острый П. при жизни больного. Этот диагноз затем был подтвержден при лапаротомии и аутопсии.
Первую успешную операцию при остром П. выполнил в 1890 г. Холстед (W. S. Halsted).
Первые монографии о хирургических заболеваниях поджелудочной железы опубликовали А. В. Мартынов в 1897 г., а затем в 1898 г. Керте (W. Korte), впервые успешно вскрывший абсцесс поджелудочной железы и рекомендовавший активную хирургическую тактику при панкреонекрозе.
Статистика
До 50-х гг. 20 в. острый П. считали редким заболеванием, обнаруживаемым лишь во время операции или при аутопсии. По данным В. М. Воскресенского (1951), отечественными учеными с 1892 по 1941 г. описано всего 200 больных острым П. С середины 50-х гг. наряду с улучшением диагностики заболевания отмечается увеличение заболеваемости острым П. При этом, по данным В.С. Маята и Ю. А. Нестеренко (1980), особенно характерен рост числа больных с деструктивными формами заболевания. Среди острых хирургических заболеваний органов брюшной полости П. занимает по частоте третье место после острого аппендицита и острого холецистита. По данным Г. Н. Акжигитова (1974), острый II. составляет 0,47% всех соматических заболеваний и 11,8% всех хирургических заболеваний. Среди больных женщин было 80,4% , мужчин — 19,6% . У больных с панкреонекрозом соотношение мужчин и женщин составляет 1 : 1. Мужчины в возрасте до 40 лет страдают П. в 2 раза чаще, чем женщины.
Этиология
Острый П. является полиэтиологическим заболеванием, возникающим вследствие повреждения ацинозных клеток поджелудочной железы, гиперсекреции панкреатического сока и затруднения оттока его с развитием острой гипертензии в протоках поджелудочной железы (панкреатических протоках), что может привести к активации ферментов в самой железе и развитию острого П.
Повреждение ацинозных клеток может происходить при закрытой и открытой травме живота, оперативных вмешательствах на органах брюшной полости, остро возникающих расстройствах кровообращения в поджелудочной железе (перевязка, тромбоз, эмболия, сдавление сосудов и др.), экзогенных интоксикациях (щелочами, к-тами и др.)? тяжелых аллергических реакциях, значительных алиментарных нарушениях и др.
Роль заболеваний желчных протоков в генезе острого П. Общепризнана. Лансеро (E. Lancereaux, 1899) высказал гипотезу о развитии острого П. вследствие забрасывания желчи в проток поджелудочной железы.
Острая желчно-панкреатическая протоковая гипертензия и рефлюкс желчи в протоки поджелудочной железы легко возникают при наличии общей ампулы для общего желчного протока и протока поджелудочной железы в случае внезапной блокады устья большого фатерова соска (сосочка двенадцатиперстной кишки), напр, желчным камнем, и др. По мнению Е. В. Смирнова с сотр. (1966), К. Д. Тоскина (1966) и др., помимо билиарно-панкреатического рефлюкса (см.), причиной возникновения острого П. может оказаться и дуоденопанкреатический рефлюкс. Если в первом случае панкреатические ферменты активируются желчью (см.), то во втором их активатором является энтеропептидаза. Затекание дуоденального содержимого в протоки поджелудочной железы оказывается возможным при зиянии большого сосочка двенадцатиперстной кишки и повышении внутри дуоденального давления.
Экспериментальные исследования Н. К. Пермякова с сотр. (1973) показали, что как избыточное употребление пищи, особенно жиров и углеводов, так и ее недостаток, особенно белков, приводит к повреждению ультраструктур ацинозных клеток даже в условиях ненарушенного оттока панкреатического секрета и способствует развитию первично-аци-нозной формы П. (метаболического П.).
Роль алиментарного фактора в развитии острого П. возрастает при приеме избыточного количества сокогонной пищи в условиях нарушения оттока панкреатического сока.
В этиологии острого П. в ряде случаев могут играть роль и другие факторы: эндокринные нарушения (гиперпаратиреоидоз, беременность, длительное лечение кортикостероидами и др.), врожденное или приобретенное нарушение жирового обмена (резко выраженная гиперлипемия), нек-рые инф. болезни (вирусный паротит и вирусный гепатит).
К предрасполагающим факторам относят аллергию. Еще П. Д. Соловое в 1937 г. объяснял происхождение панкреонекроза гиперергическим воспалением сосудов поджелудочной железы.
Впоследствии было доказано, что путем сенсибилизации животных чужеродными белками или бактерийными токсинами можно воспроизвести острый П. во всех фазах.
М. Н. Молоденков (1964) вызывалг острый П., перевязывая протоки поджелудочной железы после сенсибилизации кроликов четырехкратным подкожным введением нормальной лошадиной сыворотки.
В. В. Чаплинский и А. И. Гнаты-шак (1972) воспроизвели острый П. у собак путем сенсибилизации организма чужеродным белком и введения на этом фоне разрешающего экзогенного (пищевого) и эндогенного (метаболитного) аллергенов. Однако многочисленные модели аллергического П. далеко не идентичны аналогичному заболеванию у человека.
По данным В. И. Филина с сотр.. (1973), Г. Н. Акжигитова (1974), у больных, поступающих в хирургические стационары, наиболее часто развитию острого П. нетравматического происхождения способствуют заболевания желчных протоков и других органов пищеварения, заболевания сердечно-сосудистой системы, алиментарные нарушения, злоупотребление алкоголем и др.
Патогенез
Наибольшее распространение получила ферментативная теория патогенеза острого П.
Активация собственных ферментов^ поджелудочной железы (трипсина,, химотрипсина, эластазы, липазы., фосфолипазы и др.) в условиях повышенной функции, затрудненно го оттока панкреатического секрета и последующее ферментативное поражение ткани железы в виде отека и некроза (жирового, геморрагического, смешанного) являются наиболее характерным звеном в патогенезе острого П.
Этот процесс в поджелудочной железе идет по типу цепной реакции и начинается обычно с выделения из поврежденных клеток паренхимы железы цитокиназы. Под действием цитокиназы трипсиноген переходит в трипсин (см.). Панкреатический калликреин, активированный трипсином, действуя на кининоген, образует высокоактивный пептид — каллидин, к-рый быстро превращается в брадикинин (см. Медиаторы, аллергических реакций). Брадикинин может образоваться и непосредственно из кининогена. Под действием трипсина из различных клеток поджелудочной железы освобождаются гистамин (см.) и серотонин (см.). Через лимфатические и кровеносные пути панкреатические ферменты попадают в общее кровяное русло. В крови трипсин активирует фактор Хагемана (см. Свертывающая система крови) и плазминоген и тем самым оказывает влияние на процессы гемокоагуляции и фибринолиза.
Первоначальные патол, изменения в поджелудочной железе и других органах проявляются выраженными сосудистыми изменениями: сужение, а затем расширение сосудов, резкое повышение проницаемости сосудистой стенки, замедление кровотока, выход жидкой части крови и даже форменных элементов из просвета сосудов в окружающие ткани. Появляются серозный, серозно-геморрагический, геморрагический отек и даже массивные кровоизлияния в железе, забрюшинной клетчатке.
В условиях нарушенного местного кровообращения, тканевого обмена и непосредственного действия на клетки ферментов возникают очаги некроза паренхимы поджелудочной железы и окружающей ее жировой ткани. Этому способствует тромбооб-разование, к-рое наиболее характерно для геморрагических форм П. Из разрушенных клеток освобождаются липазы (см.). Последние, особенно фосфолипаза А, гидролизируют жиры и фосфолипиды, обусловливая жировой некроз поджелудочной железы, а распространяясь током крови и лимфы, вызывают стеатонекрозы отдаленных органов.
Общие изменения в организме обусловлены в начале энзиматической (ферментативной), а затем тканевой (из очагов некроза) интоксикацией. В связи с генерализованным воздействием на сосудистое русло вазоактивных веществ очень быстро возникают значительные расстройства кровообращения на всех уровнях: тканевом, органном и системном. Циркуляторные расстройства во внутренних органах (сердце, легкие, печень и др.) приводят к дистрофическим, некробиотическим и даже явным некротическим изменениям в них, после чего развивается вторичное воспаление.
Значительная экссудация в ткани и полости, глубокие функциональноморфологические изменения внутренних органов и другие причины вызывают выраженные нарушения водно-электролитного, углеводного, белкового и жирового обмена.
Патологическая анатомия
Патологоанатомически в основе острого П. лежат первичные деструктивные изменения ацинусов, обусловленные внутриорганной (внутриклеточной) активацией вырабатываемых поджелудочной железой пищеварительных ферментов. Развивающийся ферментный аутолиз ацинозных клеток сопровождается образованием очагов некроза и асептического (абактериального) воспаления. Поэтому отнесение острого П. к группе воспалительных процессов весьма условно; термин «панкреонекроз» точнее отражает суть патол, процесса. Инф. воспаление железы, как правило, является осложнением панкреонекроза; оно развивается в поздних стадиях заболевания вследствие микробного инфицирования очагов некроза. Лишь изредка гнойный П. может наблюдаться при септикопиемии как сопутствующее поражение вследствие метастазирования гнойной инфекции.
Общепринятой патологоанатомической классификации П. не существует. Большинство патологоанатомов различают некротическую и геморрагически-интерстициальную формы острого П., острый серозный, а также острый гнойный П.
Острый серозный П. (острый отек поджелудочной железы) чаще всего подвергается обратному развитию и лишь иногда переходит в деструктивную форму. Однако при молниеносном развитии заболевания смерть может наступить от ферментного шока в первые трое суток, когда деструкция железы еще не наступила. Эти случаи трудны для патологоанатомической диагностики, т. к. макроскопические изменения поджелудочной железы (отек) не соответствуют тяжести клин, течения. О поражении железы могут свидетельствовать лишь немногочисленные жировые некрозы (см.), обнаруживаемые в окружающей клетчатке (цветн. рис. 1). Микроскопически при этом в самой железе, как правило, обнаруживаются изменения, соответствующие диффузно-очаговому П. (цветн. рис. 2). Подобное течение П. наблюдается, как правило, при хроническом алкоголизме.
Патологоанатомические изменения железы при геморрагически-некроти-ческом П. (панкреонекрозе) зависят от масштабов поражения и продолжительности заболевания. Макроскопически в начальных фазах (1 — 3-и сут.) железа значительно увеличена в объеме (цветн. рис. 3), уплотнена, поверхность разреза имеет гомогенный желатинозный вид, дольковая структура ее строения стерта, однако четких очагов некроза еще не видно. Только под париетальной брюшиной, покрывающей поджелудочную железу (так наз. капсула), в малом и большом сальниках, капсуле почек, брыжейке кишечника можно обнаружить рассеянные мелкие желтого цвета очаги жирового некроза в сочетании с серозным и серозно-геморрагическим выпотом в полости брюшины (цветн. рис. 4).
Макроскопический вид поджелудочной железы в срок 3—7 дней от начала заболевания зависит от распространенности панкреонекроза. По масштабам поражения панкреонекроз можно разделить на три группы: диффузно-очаговый, крупноочаговый, субтотальный (тотальный).
При диффузно-очаговом панкреонекрозе в эти сроки очаги некроза диам. 0,2—1 см желтого или красноватого цвета, четко отграничены от сохранившейся паренхимы железы. Микроскопически отмечается прогрессирующий склероз некротических участков, постепенный распад лейкоцитов и смена клеточного состава воспалительного инфильтрата лимфоплазмоклеточными и гистиоцитар-ными элементами.
Очаги жирового некроза окружающей клетчатки или отсутствуют, или представлены в небольшом количестве. Капсула поджелудочной железы деструкции не подвергается.
В зонах поражения обнаруживается пролиферация мелких протоков, к-рая никогда не завершается регенерацией ацинусов. Исходом этой формы панкреонекроза является диффузно-очаговый фиброз и липоматоз поджелудочной железы.
При крупноочаговой форме П. образуется один или несколько очагов некроза размерами 2×3 — 3×4 см, имеющих в отличие от инфаркта неправильные очертания. Очаги некроза, как правило, желтого цвета и захватывают капсулу железы. Их эволюция, как и исходы заболевания, зависят от глубины поражения и локализации (головка, тело, хвост железы). Некроз хвоста железы чаще всего замещается фиброзной тканью. При некрозе тела и головки железы исход заболевания обусловлен степенью вторичных поражений стенок сосудов и крупных протоков. Крупные очаги некроза этой локализации нередко подвергаются диффузному расплавлению и секвестрации с образованием абсцесса (внут-риорганного, сальниковой сумки) или ложной кисты (см. Поджелудочная железа).
Полость кисты (цветн. рис. 5), как правило, связана с протоками железы, через к-рые происходит постоянный сброс секрета.
При прогрессирующих вариантах острого панкреатита первоначальная стадия серозного отека поджелудочной железы очень рано сменяется стадией геморрагического некроза со значительным кровоизлиянием (цветн. рис. 7) в ткани или без него. Затем следует стадия расплавления и секвестрации некротических очагов поджелудочной железы и забрюшинной клетчатки. В последней стадии нередко возникает нагноение, к-рое имеет вначале асептический характер. Обратное развитие второй стадии и переход ее в третью может осуществляться через этап образования массивного воспалительного инфильтрата в зоне железы, при к-ром в воспалительный процесс вовлекаются не только железа, но и парапанкреати-ческая забрюшинная клетчатка, и соседние органы (желудок, двенадцатиперстная кишка, селезенка и ДР-).
В большинстве случаев развитие острого П. останавливается на стадии отека или некроза, не переходя в стадию секвестрации.
Если отек и некроз поджелудочной железы и забрюшинной клетчатки при остром П. развиваются обычно в ближайшие часы заболевания, то расплавление некротических очагов начинается не ранее 3—5-го дня, а секвестрация — через 2—3 нед. и позднее от начала заболевания.
Иногда гнойное воспаление железы приобретает диффузный характер. При этом лейкоцитарные инфильтраты распространяются в строме железы по типу флегмоны (флегмонозный П.), что обычно свидетельствует о присоединении инфекции.
Стенки абсцесса сальниковой сумки образуются за счет органов, формирующих эту полость; серозные оболочки их подвергаются фиброзу. Склеротические процессы могут быть настолько интенсивны, что все полые органы верхней половины брюшной полости спаиваются в один конгломерат, затрудняющий лапаротомию. Этот конгломерат иногда принимают за опухоль. Содержимое абсцесса обычно представлено тканевым детритом, гноем и секретом поджелудочной железы. Дальнейшая эволюция абсцесса протекает в следующих основных вариантах: образование ложной кисты, эрозия стенок прилежащих органов (желудка, двенадцатиперстной, поперечной ободочной кишок) с образованием внутреннего свища, аррозия крупного артериального ствола с кровотечением в желудочно-кишечный тракт, прорыв в свободную брюшинную полость с развитием гнойного перитонита (см).
Тяжесть течения крупноочагового острого П. зависит также от масштабов жировых некрозов. При тяжелых экстраорганных поражениях наблюдается расплавление забрюшинной клетчатки с последующим формированием парапанкреатической флегмоны, распространяющейся затем по забрюшинному пространству.
Субтотальная (тотальная) форма П. обычно имеет характер геморрагического некроза и заканчивается расплавлением и секвестрацией железы с развитием осложнений, описанных выше.
Микроскопически уже в ранних фазах развития панкреонекроза обнаруживают, помимо интерстициального отека, множественные очаги жирового некроза и некроза ацинусов, расположенных преимущественно по периферии долек поджелудочной железы. В очагах некроза закономерно выявляется тромбоз капилляров, венул и пристеночный тромбоз более крупных вен (цветн. рис. 6). Расстройства гемоциркуляции во внутриорганных венах сопровождаются обширными кровоизлияниями и геморрагическим пропитыванием паренхимы железы. Степень поражения венозного русла, по-видимому, в основном и определяет как геморрагический характер некроза, так и его масштабы.
Нарушения проницаемости капилляров уже в первые 1—2 часа после деструкции ацинусов сопровождаются диапедезом лейкоцитов. В эти же сроки в отечной строме появляется большое количество тучных клеток (лаброцитов), с к-рыми связана продукция биологически активных веществ, имеющих важное значение в развитии воспалительной реакции (см. Воспаление). Через 1—2 сут. вокруг очагов некроза возникает демаркационный вал (цветн. рис. 8), состоящий из лейкоцитов и ядерного детрита. В последующем в нем выявляются гистиоциты и лимфоплазмоклеточные элементы. Особенностью эволюции панкреонекроза является быстрая активация фибробластов, сопровождающаяся интенсивным образованием коллагена с формированием соединительнотканных капсул и полей фиброза (цветн. рис. 9 —13).
При образовании кисты или абсцесса микроскопически их стенки представлены гиалинизированной фиброзной тканью с диффузно-очаговыми инфильтратами, состоящими из лимфоцитов, плазматических клеток и гистиоцитов. Внутренняя оболочка абсцесса обычно покрыта некротическим налетом и фибрином с лейкоцитарным детритом и отдельными сохранными лейкоцитами.
Электронно-микроскопические исследования поджелудочной железы, выполненные на различных моделях экспериментального П., раскрывают инициальные фазы повреждения ацинозных клеток. Прогрессирующему аутолизу ацинусов, как правило, предшествует парциальный некроз ацинозных клеток с формированием большого количества ауто-фагосом, накоплением в цитоплазме многочисленных липидных вакуолей. Эти изменения сопровождаются значительной перестройкой функции ацинозных клеток, что проявляется сменой нормального для железы мерокринового типа секреции на апокриновый и микроголокриновый, к-рым свойственна секвестрация апикальных отделов цитоплазмы вместе с гранулами секрета. Отмечается также своеобразное перебазирование гранул зимогена, содержащих весь набор синтезируемых пищеварительных ферментов, в базальные отделы цитоплазмы ацинозных клеток. При этом всякая деструкция базальной мембраны неизбежно приводит к парадоксальному выбросу секреторных гранул не в просвет канальца, а в интерстиций, откуда они могут резорбироваться в кровяное и лимф, русло. Резорбции секрета способствуют сопутствующие повреждения эндотелия капилляров и интенсивный отек стромы. Описанные изменения сопровождаются быстрой активацией калликреин-трипсиновой системы и фосфолипазы А, что приводит к прогрессирующему аутолизу с образованием очагов асептического некроза.
Клиническая картина
Выраженная боль в верхней половине живота опоясывающего характера — ведущий и наиболее постоянный симптом острого П. В ряде случаев наблюдается иррадиация болей за грудину и в область сердца. Интенсивность боли связана с раздражением рецепторов, повышением давления в общем желчном протоке и протоках поджелудочной железы, хим. воздействием трипсина.
Из-за резких болей пациенты беспокойны и постоянно меняют положение, не получая облегчения. Боли особенно выражены при геморрагическом панкреонекрозе, хотя сильные боли могут наблюдаться и при отечной фазе П. С наступлением некроза нервных окончаний интенсивность болей снижается, поэтому по интенсивности боли не всегда можно судить о степени поражения поджелудочной железы.
Тошнота и рвота — второй ведущий симптом острого П. Рвота нередко мучительная, неукротимая, не приносящая облегчения. Обычно первые ее порции содержат пищевые массы, последние — желчь и слизистое содержимое желудка. При деструктивном П. иногда вследствие возникновения острых язв желудка появляется примесь крови в рвотных массах (цвета кофейной гущи).
Кожа и слизистые оболочки при остром П. часто бледные, иногда с цианотичным оттенком. При тяжелых формах заболевания кожа холодная, покрыта липким потом. Довольно часто острый П. сопровождается механической желтухой (см.), обусловленной обтурацией общего желчного протока желчными камнями или сдавлением его воспалительным инфильтратом в головке поджелудочной железы.
Описаны патогномоничные признаки при деструктивном П.— участки цианоза кожи или подкожных кровоизлияний вокруг пупка, на боковых областях живота, передней брюшной стенке, лице.
Температура тела, в первые часы заболевания нормальная или пониженная, с присоединением воспалительных явлений повышается. Высокая температура, не имеющая тенденции к снижению, нередко является признаком деструктивного П., а позднее повышение температуры гектического характера — признаком гнойных осложнений (забрюшинная флегмона, абсцедирование).
В начале заболевания нередко наблюдается брадикардия, позже, при нарастании интоксикации, частота пульса обычно постепенно увеличивается. При отечной форме острого П. возможна артериальная гипертензия, а при деструктивной — гипотония и даже коллапс (см.).
Осложнения
Можно выделить две группы осложнений острого П.: осложнения местные, связанные с повреждением поджелудочной железы, и осложнения, обусловленные общим воздействием заболевания на организм .
Общие осложнения: печеночно-почечная недостаточность, сепсис, механическая желтуха, психоз, сахарный диабет.
Местные осложнения: перитонит (отграниченный, распространенный); забрюшинная флегмона, абсцессы брюшной полости, сальниковой сумки; некрозы стенки желудка, поперечной ободочной кишки; панкреатические свищи внутренние и наружные; ложная киста поджелудочной железы; аррозивные кровотечения.
При отечном П. осложнения наблюдаются редко. При деструктивном П. они возникают почти у каждого больного.
Печеночная недостаточность (см.) и почечная недостаточность (см.) обусловлены интоксикацией ферментативного и воспалительного генеза, гемодинамическими нарушениями, гипоксией и предшествующими нарушениями функционального состояния печени и почек.
Острые нарушения психики обусловлены интоксикацией и чаще развиваются у лиц, злоупотреблявших алкоголем. Сахарный диабет (см. Диабет сахарный) обычно возникает при деструктивном П. и разрушении всего или почти всего островкового аппарата поджелудочной железы, а у больных скрытым диабетом он может проявиться и при отечном П.
Диагноз
Физикальное исследование. Язык при остром П. обычно сухой, обложен белым или бурым налетом. При пальпации в первые часы заболевания живот резко болезненный в надчревной области, но относительно мягкий во всех отделах. Постепенно с развитием пареза жел.-киш. тракта живот увеличивается в размерах и не участвует в акте дыхания. Вначале вздутие брюшной стенки отмечается локально в надчревной области (симптом Боде), затем распространяется и на нижележащие области. Перистальтика резко ослаблена или не прослушивается, газы не отходят.
Ригидность передней брюшной стенки в надчревной области, определяемая в проекции поджелудочной железы (симптом Керте), обнаруживается почти в 60% случаев. Острый П. может сопровождаться напряжением брюшной стенки, иногда до доскообразного характера. Симптом Щеткина — Блюмберга наблюдается реже, чем ригидность передней брюшной стенки. Симптом Мейо-Робсона (болезненность в реберно-позвоночном углу) слева отмечается при вовлечении в процесс хвостового отдела поджелудочной железы и справа — при поражении ее головки.
Описаны и другие симптомы при остром П., имеющие определенное диагностическое значение: симптом Воскресенского (исчезновение пульсации аорты в надчревной области), Раздольского (болезненность при перкуссии над поджелудочной железой), Кача (гиперестезия по околопозвоночной линии слева, соответственно сегментам Thvn—ix), Махо-ва (гиперестезия выше пупка) и др.
Лабораторные методы исследования. Гематол, изменения обычно имеют место при деструктивных формах заболевания. У части больных выявляется гипохромная анемия, хотя, по данным В. В. Чаплинского, В. М. Лащевкера (1978) и др., при резком обезвоживании в первые двое суток может отмечаться эритроцитоз. Лейкоцитоз обнаруживают приблизительно у 60% больных. Характерны также нейтрофильный сдвиг влево за счет увеличения незрелых форм, лимфопения, анэозинофилия, ускорение РОЭ. Из ферментов поджелудочной железы (амилаза, липаза, трипсин) практическое значение имеет определение амилазы мочи (см. Вольгемута метод). Повышение ее активности, достигающее 8192—32768 ед. (по методу Вольгемута, при к-ром нормальные показатели не превышают 16—128 ед.), отмечается более чем у 70% больных. Однако низкая активность фермента не исключает диагноз острого П. Она может быть обусловлена склеротическими изменениями или некрозом ацинозных клеток, почечной недостаточностью, ранним или, наоборот, поздним поступлением больного. При тяжелом течении острого П. следует определять амилазу сыворотки крови, т. к. у ряда больных амилаза мочи может быть нормальной, а в крови резко повышенной и достигать 400— 500 ед. (по методу Смита—Роу, при к-ром нормальные показатели не превышают 100—120 ед.). Обычно повышается активность трипсина, а активность его ингибитора снижается. Определение активности липазы вследствие значительных колебаний ее в норме имеет меньшую диагностическую ценность. По данным А. А. Шелагурова (1970), повышение активности ферментов поджелудочной железы в крови обнаруживается у 82,5—97,2% больных. При этом важно динамическое исследование активности ферментов.
В диагностике острого П. имеет значение также уровень билирубина крови, к-рый при увеличении головки поджелудочной железы может повышаться.
Определение в крови концентрации ионов калия, натрия, кальция, а также сахара, общего белка и белковых фракций позволяет оценить тяжесть состояния больных и степень нарушения соответствующих видов обмена.
Изменения свертывающей системы крови также зависят от формы заболевания. При отечной форме и жировом панкреонекрозе, как правило, наблюдается гиперкоагуляция, при геморрагическом П.— гипокоагуляция. Почти всегда отмечается гиперфибриногенемия и повышение С-реактивного белка. По данным В. С. Савельева и соавт. (1973), Г. А. Буром-ской и соавт. (1979), изменения в кал-ликреин-кининовой системе характеризуются снижением уровня кининогена, ирекалликреина, ингибитора калликреина, к-рое наиболее выражено при деструктивном П.
Изменения показателей суточного и часового диуреза в известной мере зависят от тяжести поражения поджелудочной железы. Резкое снижение суточного и часового диуреза, анурия обычно наблюдаются при панкреонекрозе. У больных острым П. выявляются также протеинурия, микр о гематурия, цилиндрурия.
Рентгенодиагностика. При обзорном рентгенол, исследовании грудной клетки и брюшной полости обнаруживают высокое положение левой половины диафрагмы, ограничение ее подвижности, накопление жидкости в левой плевральной полости, пневматоз желудка и двенадцатиперстной кишки, парез отдельных петель тощей кишки.
При контрастном рентгенол, исследовании жел.-киш. тракта выявляют в связи с увеличением поджелудочной железы и отеком малого сальника и забрюшинной клетчатки смещение желудка кпереди, расширение двенадцатиперстной кишки, выпрямление медиального контура вертикальной ее части, увеличение так наз. желудочно-ободочного расстояния.
Компьютерная томография (см. Томография компьютерная) обнаруживает увеличение поджелудочной железы. При отечной форме острого П. тень ее имеет четкие контуры. При геморрагическом, некротическом и гнойном П. очертания железы исчезают, а тень ее становится интенсивной и неоднородной; иногда различимы полости абсцессов.
При целиакографии (см.) определяется усиленное кровенаполнение сосудов поджелудочной железы, увеличение ее объема, удлинение паренхиматозной фазы с неоднородностью тени железы. При панкреонекрозе В. И. Прокубовский (1975) отмечал ослабление или исчезновение тени внутриорганных сосудов поджелудочной железы, оттеснение вправо гастродуоденальной артерии, углообразную деформацию и оттеснение кверху общей печеночной артерии.
Специальные методы исследования. Ультразвуковая диагностика (см.) позволяет различать границы и структуру поджелудочной железы (очаговое и диффузное изменения). При интерстициальном П. выявляется увеличение размеров органа, сохраняется четкая отграниченность его от окружающих тканей, появляется передаточная пульсация с аорты. При деструктивном П. поджелудочная железа теряет однородность, контуры ее сливаются с окружающим фоном, обнаруживаются бесструктурные участки. При развитии псевдокисты определяется однородное образование с хорошо очерченной капсулой, оттесняющее соседние органы. При наличии выпота в брюшной полости эхолокация позволяет определить его уже в количестве 200 мл.
При гастроскопии (см.) и дуоденоскопии (см.), производимых обычно в трудных диагностических случаях, можно обнаружить следующие признаки острого П.: а) оттеснение задней стенки тела и привратника желудка; б) гиперемию, отек, слизь и эрозии в области оттеснения, а иногда и признаки диффузного гастрита; в) разворот петли двенадцатиперстной кишки, дуоденит, папиллит. Оттеснение задней стенки желудка в сочетании с выраженными воспалительными изменениями являются признаками абсцесса сальниковой су мкм.
Большое значение в диагностике острого П. имеет лапароскопия (см. Перитонеоскопия), к-рая позволяет достоверно диагностировать наиболее тяжелую форму заболевания — панкреонекроз.
Лапаросквпическими признаками панкреонекроза являются бляшки очаговых некрозов жировой ткани, обнаруживаемые на большом и малом сальниках, желудочно-ободочной связке, иногда на брюшине передней брюшной стенки, круглой связке печени, брыжейках поперечной ободочной и тонкой кишок.
Вторым признаком панкреонекроза является наличие экссудата в брюшинной полости. При жировом панкреонекрозе он имеет серозный характер. Количество экссудата бывает различным — от 10—15 мл до нескольких литров. Доказательством панкреатогенной природы такого перитонита является резкое повышение активности панкреатических ферментов в экссудате. Исследование активности трипсина и липазы в экссудате имеет меньшее значение.
Частым признаком панкреонекроза является серозное пропитывание жировой клетчатки (так наз. стекловидный отек).
Геморрагический панкреонекроз отличается наличием экссудата красного цвета — от буровато-коричневого до явно геморрагического. Иногда видны очаги кровоизлияний в желудочно-ободочной связке или большом сальнике.
В отличие от панкреонекроза отечный П. обычно не имеет характерных лапароскопических данных, т. к. патол, процесс, как правило, не выходит за пределы сальниковой сумки. Однако в ряде случаев в брюшной полости обнаруживают серозный выпот с высокой активностью ферментов.
Дифференциальный диагноз острого П. проводят с острым холециститом (см.), холецистопанкреатитом (см.), прободной язвой желудка и двенадцатиперстной кишки (см. Язвенная болезнь), острым аппендицитом (см.), острой кишечной непроходимостью (см. Непроходимость кишечника), инфарктом кишечника (см.), острым гастритом (см.), пищевой токсикоинфекцией (см. Токсикоинфекции пищевые), инфарктом миокарда (см.).
Дифференциация отечной и деструктивной форм П., подлежащих различному лечению, остается затруднительной. Как отечная, так и деструктивная форма П. нередко начинаются одинаково. Однако уже через несколько часов после проведения интенсивной терапии клин, проявления при отечном П. стихают, состояние больного улучшается. Симптоматика деструктивного П., несмотря на проводимую терапию, длительно сохраняется, состояние больного улучшается незначительно. При прогрессировании процесса оно ухудшается: усиливается тахикардия, нарастают интоксикация и перитонеальные явления. При тотальном панкреонекрозе с первых часов заболевания развивается тяжелая клин, картина (заостренные черты лица, частый малый пульс, олигурия).
В трудных для диагностики случаях становятся необходимыми лапароскопия и другие инструментальные методы исследования.
Разработаны критерии, к-рыми следует руководствоваться при дифференциальной диагностике различных форм II. (табл.).
Лечение
При тяжелом состоянии больного леч. мероприятия следует начинать еще на догоспитальном этапе. Они должны быть направлены на борьбу с резко выраженным болевым синдромом и артериальной гипотензией, т. е. включать элементы инфузионной терапии (полиглюкин, гемодез и др.), а также применение сердечных гликозидов, аналептиков, стимулирующих дыхание, анальгетиков, кроме наркотических.
Госпитализация больных острым П. должна производиться только в хирургический стационар. Характер леч. мероприятий, проводимых в стационаре, зависит от выраженности клин, картины заболевания, тяжести состояния больного, данных лабораторно-инструментальных методов исследования.
Лечение отечной формы острого П., в большинстве случаев не сопровождающейся тяжелой интоксикацией, должно быть комплексным. В первую очередь оно направлено на создание функц, покоя поджелудочной железы, что обеспечивается голодом (3—5 дней), назначением льда на надчревную область, приемом щелочных р-ров, чрезназальным дренированием желудка и двенадцатиперстной кишки, подавлением ферментативной активности железы, для чего назначают холинолитики (атропин, Скополамин, платифиллин), производные пиримидина (метилурацил, пентоксил).
Предупреждение и ликвидация явлений желчной и панкреатической гипертензии достигаются с помощью спазмолитиков (нитроглицерина, папаверина, но-шпы, эуфиллина), внутривенного введения новокаина.
Устранения боли и различных нейрорефлекторных расстройств достигают назначением анальгетиков, спазмолитиков, ганглиоблокаторов (пентамина, бензогексония и др.), а также паранефральной блокады (см. Новокаиновая блокада) или блокады круглой связки печени.
Для уменьшения проницаемости сосудистой стенки назначают антигистаминные препараты (димедрол, пипольфен и др.). Лечение больных, находящихся в тяжелом состоянии, с выраженной токсемией, характерной, как правило, для деструктивных форм острого П., должно проводиться в палате интенсивной терапии или реанимационном отделении совместно с хирургом, реаниматологом, терапевтом.
Леч. мероприятия, проводимые при тяжелых формах заболевания, должны быть направлены на блокаду ферментообразующей функции поджелудочной железы, выведение панкреатических ферментов и интенсивную дезинтоксикацию организма, профилактику гнойных осложнений.
Блокада экскреторной функции поджелудочной железы может осуществляться назначением голода, атропина и местного холода. При тяжелом течении заболевания более эффективны локальная гипотермия железы или введение цитостатиков.
Охлаждение поджелудочной железы проводят путем локальной желудочной гипотермии (см. Гипотермия искусственная, локальная) с помощью длительного промывания желудка холодной водой (открытый метод) или специальных охлаждающих аппаратов АГШ-1 и др. (закрытый метод). Гипотермия позволяет в значительной мере подавить экскреторную функцию клеток железы. Однако длительность процедуры (4—6 час.), частое возникновение осложнений со стороны легких, выраженные нарушения кислотно-щелочного равновесия вследствие потерь желудочного сока при открытом методе ограничивают применение гипотермии в клин, практике, особенно у больных пожилого и старческого возраста.
С начала 70-х гг. все более широкое применение для лечения острого П. находят различные цитостатики (5-фторурацил, циклофосфан, фторафур). Наиболее эффективно применение цитостатиков при регионарном введении в чревный ствол после катетеризации его по Сельдингеру — Эдману, что позволяет снизить дозу вводимого препарата, одновременно значительно повысив концентрацию его в тканях поджелудочной железы.
По данным Джонсона (R. М. Johnson, 1972), А. А. Карелина и соавт. (1980), механизм леч. действия цитостатиков при остром П. заключается в ингибировании экскреторной функции клеток поджелудочной железы. Экспериментальными исследованиями Ю. А. Нестеренко и сотр. (1979) установлено, что Внутриартериальное введение фторурацила в дозе 5 мг на 1 кг веса вызывает снижение внешнепанкреатической секреции на 91% и является оптимальной леч. дозой. При внутривенном введении эта доза может быть увеличена в 2—3 раза. Применение цитостатиков показано при деструктивном П. Нецелесообразно их применение у больных с тотальным панкреонекрозом, гнойными осложнениями П. и почечно-печеночной недостаточностью.
Выведение панкреатических ферментов и дезинтоксикация организма осуществляется с помощью методов внутривенного или Внутриартериальное введения диуретиков (для форсированного диуреза), перитонеального диализа и дренирования грудного лимф, протока.
При форсированном диурезе панкреатические ферменты, компоненты кининовой системы, а также нек-рые продукты клеточного распада выводятся почками. Методика форсированного диуреза включает водную нагрузку, введение диуретиков, коррекцию электролитного и белкового баланса. Основными компонентами вводимой жидкости могут быть 5 — 10% р-р глюкозы, р-р Рингера, реополиглюкин, солевой р-р. При внутривенном методе вводят ежесуточно 5 — б л жидкости на протяжении 3—10 сут. Форсирование диуреза осуществляют путем введения после инфузии каждых 2 л жидкости мочегонных препаратов (лазикса, маннитола) и добиваются, чтобы суточный диурез достигал 3V2—4 д.
По данным Г. А. Буромской и сотр. (1980), Внутриартериальное введение диуретиков более эффективно ликвидирует вне- и внутриклеточную гидратацию, не повышает центральное венозное давление, не вызывает гиперволемию. В то же время при этом методе токсические продукты выводятся непосредственно из клеток поджелудочной железы, что обусловливает более выраженный дезинтоксикационных! эффект. Объем вводимой внутриартериаль-но жидкости зависит от интоксикации и степени дегидратации больного и составляет в среднем 4—5 л в сутки. Продолжительность внут-риартериального введения жидкости обычно составляет 3—4 сут. При проведении форсированного диуреза необходим контроль за центральным венозным давлением, гематокритом, средним диаметром эритроцитов, показателями объема циркулирующей крови, кислотно-щелочным равновесием, уровнем электролитов.
Важную роль в борьбе с ферментативной токсемией играют антифер-ментные препараты (трасилол, контрикал, тзалол, пантрипин, гордокс и др.). Их необходимо вводить в больших дозах в течение 3—5 дней.
Дренирование грудного лимф, протока (см. Грудной проток) осуществляют при деструктивных формах панкреатита с целью выведения из организма ферментов поджелудочной железы.
Количество удаляемой лимфы зависит от степени интоксикации и возможностей заместительной терапии. Лимфу, очищенную от токсических продуктов и панкреатических ферментов путем фильтрации через ионообменные колонки (см. Лимфосорбция), реинфузируют в вену. По данным В. М. Буянова и сотр. (1979), перспективным методом дезинтоксикации организма при остром П. является внутривенная жидкостная лимфостимуляция.
Перитонеальный диализ (см.) показан при обнаружении в брюшной полости во время лапароскопии или лапаротомии большого количества серозного или геморрагического выпота. В зависимости от функции дренажей и состояния больного диализ продолжают 2—4 дня.
Профилактику и лечение тромбоэмболических осложнений производят под контролем показателей тромбоэластограммы и коагулограммы. При деструктивном П. уже в первые часы заболевания при наличии высокой фибринолитической активности и гипертрипсинемии для профилактики распространенного внутрисосудистого свертывания крови целесообразно, кроме антиферментов, вводить также гепарин, низкомолекулярные р-ры (5% р-р глюкозы, гемодез, реополиглюкин, поливинол, неокомпенсан и др.).
Коррекцию электролитного обмена производят введением изотонического или 10% р-ра хлорида натрия, 10% р-ра хлорида калия, 1% р-ра хлорида кальция, р-ра Рингера — Локка и др. При нарушении углеводного обмена вводят необходимые дозы глюкозы и инсулина. С целью коррекции белкового обмена переливают кровь, плазму, аминон, альбумин.
Для профилактики гнойных осложнений, особенно в фазе расплавления и секвестрации некротических очаго-в в поджелудочной железе, применяют антибиотики широкого спектра действия (канамицин, гентамицин, мономицин, цепорин и др-).
По данным В. С. Савельева (1977), наиболее эффективно введение антибиотиков в чревный ствол.
При некротических формах П. необходимо также стимулировать репаративные процессы в поджелудочной железе и других органах. Для этого назначают пентоксил, метилурацил, анаболические гормоны.
Все операции при остром П. целесообразно разделять на три группы: 1) экстренные и срочные, выполняемые в первые часы и дни заболевания; 2) отсроченные, к-рые производят в фазе расплавления и секвестрации некротических очагов поджелудочной железы и забрюшинной клетчатки, через 10—14 дней и позднее от начала болезни; 3) плановые, выполняемые в период полного прекращения острого воспаления в поджелудочной железе, через 4—6 нед. от начала приступа, после завершения обследования больного (эти операции предназначены для профилактики рецидива острого П.).
Показания к экстренным и срочным операциям: разлитой ферментативный перитонит; острый П., обусловленный холедохолитиазом (обтурацией большого сосочка двенадцатиперстной кишки).
При экстренных и срочных операциях после лапаротомии через верхнесрединный разрез (см. Лапаротомия) производят ревизию брюшной полости, выясняя состояние поджелудочной железы, забрюшинной клетчатки, париетальной брюшины и желчевыводящих путей.
При отечном П. в брюшной полости иногда обнаруживают серозный или желчный выпот. Поджелудочная железа увеличена в объеме, плотна на ощупь, на бледной или матовой поверхности ее видны точечные кровоизлияния. При геморрагическом панкреонекрозе обнаруживаются кровянистый выпот, нередко с гнилостным запахом, часто с примесью желчи, при гнойном П.— мутный выпот с фибрином. Поджелудочная железа при ранней стадии геморрагического панкреонекроза увеличена, поверхность ее покрыта множественными кровоизлияниями. При тотальном панкреонекрозе она бурого или черного цвета, на большом и малом сальнике, париетальной брюшине, брыжейке тонкой и толстой кишок и других органах часто видны очаги стеатонекроза.
Выпот с примесью желчи, пропитывание ею печеночно-дуоденальной связки, увеличение размеров желчного пузыря, расширение общего желчного протока свидетельствуют о П., осложненном желчной гипертензией.
При отечном П. после удаления выпота брюшную полость обычно зашивают наглухо после обкалывания железы р-ром новокаина с антибиотиками и антиферментными препаратами.
При выраженной геморрагической или желчной имбибиции забрюшинной клетчатки производят широкое вскрытие забрюшинного пространства вокруг железы и в боковых каналах живота (околоободочноки-шечных бороздах, Т.). Операцию заканчивают дренированием сальниковой сумки, иногда в сочетании с оментопанкреатопексией, или дренированием брюшинной полости с последующим перитонеальным диализом.
При обширном геморрагическом панкреонекрозе А. А. Шалимов с сотр. (1978), В. И. Филин с сотр. (1979), Холлендер (L. F. Hollender, 1976) и др. производят резекцию поджелудочной железы, чаще всего левостороннюю.
При остром П., протекающем с желтухой, обусловленной холедохолитиазом, производят холедохотомию (см.), удаляют камни, заканчивая операцию наружным дренированием общего желчного протока (см. Дренирование). При вклиненных камнях большого сосочка двенадцатиперстной кишки производят пластику большого сосочка двенадцатиперстной кишки — трансдуоденальную папиллосфинктеропласти-ку (см. Фатеров сосок).
В фазе расплавления и секвестрации некротических очагов поджелудочной железы производят некрэктомии) и секвестрэктомию.
Некрэктомия возможна не ранее чем через 2 нед. от начала заболевания, т. к. зона некроза железы четко определяется не ранее 10-го дня с момента приступа острого П. Секвестр Эктомия, т. е. удаление отторгнувшихся некротизированных участков железы и забрюшинной клетчатки, возможна обычно не ранее 3—4-й нед. от начала заболевания.
Операция в фазе расплавления и секвестрации заключается в широком вскрытии сальниковой сумки через желудочно-ободочную связку, в ревизии железы и забрюшинной клетчатки, удалении некротизированных тканей, дренировании и тампонаде сальниковой сумки и забрюшинного пространства. После операции через дренажи осуществляют активную аспирацию гнойного отделяемого.
Плановые операции направлены в основном на санацию желчного пузыря и протоков (холецистэктомия, холе дохо л итотомия, холедоходуодено-стомия и др.) и лечение заболеваний других органов пищеварения, служащих причиной рецидива острого П. (язвенной болезни желудка, двенадцатиперстной кишки, дивертикулов двенадцатиперстной кишки, дуоденостаза и др.).
В послеоперационном периоде продолжают комплексное консервативное лечение острого П.
Тампоны из сальниковой сумки меняют на 7—8-й день, стараясь формировать широкий раневой канал, к-рый периодически промывают антисептическими р-рами (фурацилина, риванола, йодинола).
В фазе секвестрации могут возникать аррозивные кровотечения.Иногда они могут быть обусловлены нарушениями свертывающей системы крови. При профузных кровотечениях производят обшивание и перевязку сосудов в ране или на протяжении или их эмболизацию, тампонаду или резекцию поджелудочной железы. При фибринолитических кровотечениях показаны прямые гемотрансфузии (см. Переливание крови) и введение ингибиторов фибринолиза — е-аминокаироновой к-ты, антиферментов и др.
Свищи поджелудочной железы возникают вследствие продолжающейся гнойной деструкции ее или после операции по поводу панкреонекроза. В большинстве случаев при консервативном лечении, особенно при применении рентгенотерапии, свищи заживают в течение нескольких недель или месяцев. Если количество отделяемого из свища в течение 2—3 мес. не уменьшается, показано оперативное лечение.
Ложная киста поджелудочной железы также образуется вследствие локального некроза органа. При этом через разрушенные выводные протоки продолжается секреция панкреатического сока в очаг деструкции, к-рый отграничивается вновь образуемой соединительной тканью, постепенно образующей стенку кисты. Псевдокиста поджелудочной железы может нагноиться, перфорировать или, сдавливая соседние органы, вызывать непроходимость кишечника, общего желчного протока. Методом выбора при оперативном лечении постнекро-тических псевдокист является пан-креатоцистоэнтеро- и панкреатоци-стогастроанастомоз. При дистальном расположении кисты показана резекция поджелудочной железы; при нагноении кисты производят марсупиализацию (см.).
Прогноз и Профилактика
Прогноз при остром П. всегда серьезен. Общая летальность составляет от 3 до 7 % , а летальность при панкреонекрозе — от 20 до 50%. В случаях панкреонекроза, потребовавших оперативного лечения, летальность колеблется от 30 до 85% .
Отдаленные результаты лечения острого II. у 50% больных хорошие, более чем у 30% — удовлетворительные, у 15—20% развивается хрон. П.
Профилактика. Целесообразна диспансеризация больных, перенесших острый П, Учитывая важную роль заболеваний желчных путей в возникновении острого П., санация их является эффективной мерой профилактики рецидива заболевания. Необходимо также соблюдение диеты и исключение злоупотребления алкоголем. В период ремиссии рекомендуют сан.-кур. лечение в санаториях жел.-киш. профиля (Боржоми, Железноводск, Трускавец, Краинка, Кар лови Вари).
Особенности острого панкреатита в пожилом и старческом возрасте. Пациенты пожилого и старческого возраста составляют более 25% больных острым П. Это объясняется прежде всего увеличением количества людей этого возраста среди населения. Немаловажное значение имеют также возрастные изменения в поджелудочной железе, в частности такие, как деформация протоков с облитерацией и расширением их, за-пустевание кровеносной капиллярной сети, фиброз междольковых перегородок и др. Способствуют более частому развитию острого П. и функц, нарушения органов пищеварения, характерные для этого возраста, а также часто встречающиеся заболевания печеночных и желчных протоков, желудка, двенадцатиперстной и толстой кишок, сердечно-сосудистой системы.
Наряду с обычной патоморфол, картиной заболевания у больных этой возрастной группы нередко наблюдается апоплексия поджелудочной железы или массивные жировые некрозы при липоматозе стромы железы.
Клин, проявления острого П. в этой группе больных характеризуются рядом особенностей. В связи с частым наличием у них разнообразных сопутствующих заболеваний даже легкие формы острого П. нередко протекают с выраженным нарушением функций жизненно важных органов и систем. Поэтому течение заболевания чаще сопровождается развитием острой сердечнососудистой, дыхательной, печеночно-почечной недостаточности, различных видов энцефалопатий и нарушением инкреторной функции поджелудочной железы. Это проявляется желтухой, олиго- и анурией, гипо- или гипергликемией. В то же время характерна незначительная болезненность при пальпации в надчревной области и выраженный парез жел.-киш. тракта. Комплексное консервативное лечение острого Г1. у больных пожилого и старческого возраста должно обязательно включать меры по лечению сопутствующих заболеваний, в первую очередь сердечно-сосудистой и дыхательной систем, профилактику и лечение печеночно-почечной недостаточности,, нарушений углеводного обмена. В связи с этим лечение таких больных проводят в палате интенсивной терапии или реанимационном отделении.
Особенности острого панкреатита у детей
Острый П. у детей встречается редко. Этиология заболевания весьма разнообразна (некоторые инфекционные болезни, аллергические состояния и др.). В большинстве случаев этиол, факторы остаются неясными; в связи с этим у детей внезапно возникающие острые П. принято называть идиопатическими.
Заболевание часто начинается с общего недомогания ребенка, отказа от пищи и подвижных игр. Развивающаяся затем клин, картина в известной мере зависит от формы острого П.
Острый отек поджелудочной железы у детей (особенно младшей возрастной группы) протекает сравнительно легко, симптомы менее выражены, чем у взрослых, и часто расцениваются педиатрами как «интоксикация неясной этиологии». Проводимое симптоматическое лечение приводит к быстрому улучшению общего состояния. Только специальное обследование позволяет поставить правильный диагноз. У детей старшего возраста заболевание начинается с острых болей в животе, вначале разлитых, а затем локализующихся в надчревной области или носящих опоясывающий характер. Реже наблюдается постепенное нарастание болей. Одновременно появляются многократная рвота, обильное слюноотделение. Ребенок принимает вынужденное положение, чаще на левом боку. Температура тела нормальная или субфебрильная, язык влажен, умеренно обложен белым налетОхМ. Пульс удовлетворительного наполнения, ритмичен, учащен, АД нормальное или слегка понижено. При осмотре отмечается бледность кожных покровов. Живот правильной формы, не вздут, участвует в акте дыхания. Пальпация передней брюшной стенки безболезненна, живот мягкий. Такое несоответствие между жестокими болями в животе и отсутствием объективных данных, говорящих о наличии острого заболевания органов брюшной полости, характерно именно для отечной формы острого II. В крови отмечается умеренный лейкоцитоз, без значительного изменения формулы. Наиболее информативным и ранним диагностическим признаком является повышение активности амилазы в крови. Несколько позже повышается содержание амилазы в моче. Как правило, наблюдается умеренная гипергликемия.
Геморрагический и жировой некроз сопровождается выраженной симптоматикой и тяжелым течением. У детей младшего возраста заболевание проявляется быстро нарастающим беспокойством. Ребенок кричит и мечется от болей, принимает вынужденное положение. Постепенно двигательное беспокойство сменяется адинамией. Дети старшего возраста обычно указывают на локализацию болей в верхних отделах живота, их опоясывающий характер, иррадиацию в надключичную область, лопатку. Появляется многократная рвота, изнуряющая ребенка. Общее состояние прогрессивно ухудшается. Кожные покровы бледны, с цианотичным оттенком. Развиваются эксикоз, тяжелая интоксикация. Язык сухой, обложен. Пульс частый, иногда слабого наполнения, АД постепенно снижается. Температура тела обычно субфебрильная, в редких случаях повышается до 38—39°.
При гнойном П. в начале заболевания еще более выражено несоответствие между субъективными признаками острого живота и отсутствием или малой выраженностью объективных данных. /Кивот у ребенка активно участвует в акте дыхания. Перкуссия и пальпация незначительно болезненны. Напряжение мышц передней брюшной стенки выражено слабо. Затем развивается парез кишечника, болезненность при пальпации усиливается, появляются симптомы раздражения брюшины» Температура тела повышается, характерен значительный лейкоцитоз. Наступает нарушение водно-электролитного баланса, повышается количество сахара в крови. Резко нарастает концентрация амилазы в крови и моче. Снижение ее уровня является плохим прогностическим признаком.
Иногда у детей младшего возраста тяжелый геморрагический или жировой некроз проявляется клин, картиной острого прогрессирующего асцита.
Рентгенол, исследование у детей, как правило, мало информативно.
У детей старшего возраста при обоснованном подозрении на панкреонекроз можно применить лапароскопию.
Дифференциальный диагноз острого П. у детей проводят с острым аппендицитом, кишечной непроходимостью и перфорацией полых органов.
Лечение острого П. у детей преимущественно консервативное. Всем детям после установления диагноза назначают комплекс леч. мероприятий, направленных на борьбу с болевым синдромом, интоксикацией и вторичной инфекцией. Важной задачей является создание функц, покоя поджелудочной железы, блокада ее ферментообразующей функции, борьба с нарушениями водно-электролитного баланса.
Комплексное консервативное лечение у детей при остром П., диагностированном в ранние сроки (1—2-е сутки), обычно приводит к выздоровлению.
При четких клин, признаках гнойного П. или перитонита показано оперативное вмешательство. У детей дошкольного возраста сложность дифференциальной диагностики часто приводит к необходимости распознавать острый П. во врвхмя лапаротомии, производимой по поводу предполагаемого острого аппендицита или другого заболевания. Оперативное лечение проводят по тем же принципам, что и у взрослых.
Все дети, переболевшие острым П., нуждаются в длительном (до 2 лет) диспансерном наблюдении у хирурга и эндокринолога.
Хронический панкреатит
Хрон. П. встречается часто — по секционным данным, от 0,18 до 6% случаев. Однако в клин, практике это заболевание, по-видимому, встречается еще чаще, но не всегда диагностируется. Обычно хрон. П. выявляется в среднем и пожилом возрасте, несколько чаще у женщин, чем у мужчин. Хрон. П. у детей встречается редко.
Различают первичный хрон. П., при к-ром воспалительный процесс с самого начала локализуется в поджелудочной железе, и так наз. вторичный, или сопутствующий, П., постепенно развивающийся на фоне других заболеваний жел.-киш. тракта, напр, язвенной болезни, гастрита, холецистита и др.
Этиология и патогенез
Этиология первичного хрон. П. разнообразна. В хрон, форму может перейти тяжелый или затянувшийся острый П. Но чаще хрон. П. возникает постепенно под воздействием таких факторов, как бессистемное нерегулярное питание, частое употребление острой и жирной пищи, хрон, алкоголизм, особенно в сочетании с дефицитом в пище белков и витаминов. По данным Бенсона (J. A. Benson), в США хрон, рецидивирующий П. в 75% случаев возникает у больных, страдающих хрон. алкоголизмом. Пенетрация язвы желудка или двенадцатиперстной кишки в поджелудочную железу также может привести к развитию хрон, воспалительного процесса в ней. Среди других этиол, факторов следует назвать хрон, нарушения кровообращения и атеросклеротическое поражение сосудов поджелудочной железы, инф. болезни, экзогенные интоксикации. Иногда П. возникает после операций на желчных путях или желудке. Более редкой причиной является поражение поджелудочной железы при узелковом периартериите, тромбоцитопенической пурпуре, гемохроматозе, гиперлипемии. В ряде случаев, по данным нек-рых исследователей, в 10—15% причина хрон. П. остается неясной. Предрасполагающими факторами в возникновении хрон. П. являются также препятствия для выделения панкреатического сока в двенадцатиперстную кишку, вызванные спазмом или стенозом ампулы сфинктера Одди, а также недостаточностью его, к-рая облегчает попадание дуоденального содержимого в проток поджелудочной железы.
Одним из ведущих механизмов развития хрон. воспалительного процесса в поджелудочной железе является задержка выделения и внутриорганная активация панкреатических ферментов, в первую очередь трипсина и липазы (фосфолипазы А), осуществляющих аутолиз паренхимы железы. Активация эластазы и нек-рых других ферментов ведет к поражению сосудов поджелудочной железы. Действие кининов на мельчайшие сосуды приводит к развитию отека. Гидрофильный эффект продуктов распада в очагах некроза ткани поджелудочной железы также способствует отеку, а в последующем — образованию ложных кист. В развитии, особенно прогрессировании хрон. воспалительного процесса, большое значение имеют процессы аутоагрессии.
При хрон, гастрите (см.) и дуодените (см.) нарушается выработка энтерохромаффинными клетками с лизис-той оболочки желудка и двенадцатиперстной кишки полипептидных гормонов, к-рые участвуют в регуляции секреции поджелудочной железы.
При хрон. П. инф. происхождения возбудитель может проникнуть в поджелудочную железу из двенадцатиперстной кишки (напр., при дисбактериозе, энтеритах) или из желчных путей (при холецистите, холангите) через протоки поджелудочной железы восходящим путем, чему способствуют дискинезии жел.-киш. тракта, сопровождающиеся дуоденопанкреатическим и холе-дохопанкреатическим рефлюксом.
Патологическая анатомия
Патологоанатомически хрон. П. подразделяют на хрон, рецидивирующий П. и хрон, склерозирующий П.
Хрон, рецидивирующий П. по существу является пролонгированным вариантом острого мелкоочагового панкреонекроза, поскольку всякий рецидив болезни сопровождается образованием свежих очагов некроза паренхимы поджелудочной железы и окружающей жировой клетчатки.
Макроскопически в период обострения железа представляется несколько увеличенной в объеме и диффузно уплотненной. Микроскопически в ней обнаруживаются свежие и организующиеся очаги некроза паренхимы и жировой клетчатки, чередующиеся с рубцовыми полями, очагами обызвествления, мелкими псевдокистами, лишенными эпителиальной выстилки. Отмечается также значительная деформация и расширение просвета выводных протоков, содержащих уплотненный секрет и нередко микролиты. В ряде случаев наблюдается диффузно-очаговое обызвествление интерстиция, и тогда говорят о хрон, кальцифицирующем П.
Воспалительная инфильтрация из лейкоцитов наблюдается лишь в очагах свежего некроза паренхимы. Она постепенно стихает по мере организации очагов деструкции, сменяясь диффузно-очаговыми инфильтратами из лимфоидных, плазматических клеток и гистиоцитов. Многие исследователи считают эти инфильтраты проявлением аутоиммунной реакции замедленного типа, возникающей в ответ на постоянное антигенное воздействие из очагов деструкции ацинусов.
Хрон, склерозирующий П. отличается диффузным уплотнением и уменьшением поджелудочной железы в размерах. Ткань железы приобретает каменистую плотность и макроскопически напоминает опухоль. Микроскопически обнаруживают диффузный фокальный и сегментарный склероз с прогрессирующим разрастанием соединительной ткани вокруг протоков, долек и внутри ацинусов. Причиной склероза является постоянная убыль паренхимы, протекающая по типу некроза или атрофии отдельных ацинусов и групп ацинусов. В далеко зашедших случаях на фоне диффузного фиброза с трудом обнаруживаются небольшие островки атрофичной паренхимы. Наряду с этим отмечается выраженная пролиферация эпителия протоков с образованием аденоматозных структур, к-рые иногда трудно дифференцировать с аденокарциномой. В просветах расширенных выводящих протоков постоянно встречаются сгущенный секрет, кристаллические отложения извести, микролиты. В окружности протоков обнаруживается большое количество гиперплази-рованных панкреатических островков (Лангерганса). Новообразования ацинусов не происходит, некроз паренхимы железы замещается рубцом.
Как и при рецидивирующей форме П., среди полей фиброзной ткани можно обнаружить лимфоплазмоцитарные инфильтраты, являющиеся отражением аутоиммунных процессов. При этом морфологически в поджелудочной железе преобладают не некротические, а дист-рофически-атрофические изменения ацинусов с медленным их замещением соединительной тканью.
При всех вариантах хрон. П. наблюдаются одинаковые осложнения. Чаще всего встречается рубцовая стриктура протока поджелудочной железы, а также закупорка его камнем или аденоматозным полипом. При этом возможна обтурация общего желчного протока с развитием механической желтухи. Иногда наблюдается тромбоз селезеночной вены. Нередко на фоне хрон. П. развивается сахарный диабет, хотя в отличие от ацинусов островки Лангерганса хорошо регенерируют, и среди рубцовой ткани их всегда можно обнаружить.
Клиническая картина
Клиническая картина хрон. П. весьма вариабельна, но в большинстве случаев включает следующие симптомы: боль в надчревной области и левом подреберье; диспептические явления; так наз. панкреатогенные поносы; похудание, гипопротеинемию, симптомы полигиповитаминоза; признаки сахарного диабета.
Боль локализуется в надчревной области справа (при преимущественной локализации процесса в области головки поджелудочной железы); при вовлечении в воспалительный процесс ее тела боль наблюдается в надчревной области; при поражении ее хвоста — в левом подреберье. Нередко боль иррадиирует в спину (на уровне X —XII грудных позвонков) или имеет опоясывающий характер, усиливается в положении больного лежа на спине и может ослабевать в положении сидя, особенно при небольшом наклоне вперед. Боль может иррадиировать также в область сердца, имитируя стенокардию, в левую лопатку, левое плечо, а иногда в левую подвздошную область. Интенсивность и характер болей различны; они могут быть постоянными (давящими, ноющими), появляться через нек-рое время после еды (как при язвенной болезни), особенно после приема жирной или острой пищи, или быть приступообразными по типу панкреатической колики.
Диспептические симптомы (панкреатическая диспепсия) встречаются часто, особенно при обострении заболевания или тяжелом течении болезни. Многие больные отмечают также потерю аппетита, отвращение к жирной пище. В то же время при развитии сахарного диабета больные могут ощущать сильный голод и жажду. Часто наблюдаются повышенное слюноотделение, отрыжка, тошнота, рвота, метеоризм. Стул в легких случаях нормальный, в более тяжелых наблюдается склонность к поносам или чередование запоров и поносов. Однако в типичных далеко зашедших случаях хрон. П. (при наличии явных признаков, внешнесекреторной недостаточности поджелудочной железы) более характерными являются панкреатические поносы с выделением обильного кашицеобразного зловонного с жирным блеском кала.
Вследствие развития внешнесекреторной недостаточности поджелудочной железы и нарушения процессов переваривания и всасывания в кишечнике нарастает похудание. Ему способствует обычно наблюдавшаяся у больных потеря аппетита, а также присоединение сахарного диабета.
При тяжелых формах заболевания возможны депрессия, ипохондрия и другие психические нарушения. При алкогольном П. нарушения психики могут быть обусловлены длительным действием алкоголя на ц. н. с.
Течение заболевания обычно имеет затяжной характер. Выделяют 5 форм заболевания: 1) рецидивирующая форма, характеризующаяся отчетливыми периодами ремиссии и обострений процесса; 2) болевая форма, протекающая с постоянными болями, доминирующими в клинической картине; 3) псевдоопухолевая форма; 4) латентная (безболевая) форма; 5) склерозирующая форма, для к-рой характерны рано возникающие и прогрессирующие признаки недостаточности функций поджелудочной железы. При последней форме иногда наблюдается механическая желтуха вследствие сдавления общего желчного протока склерозированной головкой поджелудочной железы. Т. Г. Ренева с сотр. (1978) выделяет 3 формы течения хрон. П.: легкую, среднетяжелую и тяжелую. Последняя протекает с упорными поносами, дистрофическими расстройствами, нарастающим истощением.
Осложнения: кисты, кальцификаты поджелудочной железы, сахарный диабет, тромбоз селезеночной вены, стеноз протока поджелудочной железы. На фоне длительного хрон. П1. возможно развитие рака подже-лудочной железы.
Диагноз
Физикальное исследование. При пальпации живота у больных хрон. П. обычно характерна болезненность в надчревной области и левом подреберье. Рядом исследователей описаны болевые точки и зоны, болезненность в к-рых особенно характерна. Так, при поражении головки поджелудочной железы боль может отмечаться при давлении в так наз. панкреатической точке Дежардена, располагающейся в области проекции на переднюю брюшную стенку дистального отдела протока поджелудочной железы (приблизительно на расстоянии 5—7 см от пупка по линии, соединяющей пупок с правой подмышечной впадиной), или в более широкой холедохопанкреатической зоне Шоффара, располагающейся между указанной выше линией, передней срединной линией тела и перпендикуляром, опущенным на последнюю линию из точки Дежардена. Нередко отмечается болезненность точки в реберно-позвоночном углу (симптом Мейо-Робсона). Иногда отмечается зона кожной гиперестезии соответственно зоне иннервации 8 —10-го грудного сегмента слева (симптом Кача) и нек-рая атрофия подкожной клетчатки в области проекции поджелудочной железы на переднюю брюшную стенку, описанная А. А. Шела-гуровым (1970). Пропальпировать увеличенную и уплотненную поджелудочную железу при хрон. П. удается очень редко.
Нек-рое диагностическое значение может иметь аускультация надчревной области при полном выдохе: иногда слышен систолический шум, к-рый возникает вследствие сдавления брюшной части аорты увеличенной и уплотненной поджелудочной железой.
Лабораторные методы исследования нередко выявляют у больных хрон. П. умеренную гипохромную анемию, ускорение РОЭ, нейтрофильный лейкоцитоз, диспротеинемию за счет повышенного содержания глобулинов, повышение активности трансаминаз и альдолазы в сыворотке крови. При поражении островкового аппарата поджелудочной железы выявляется гипергликемия (см.) и гликозурия (см.), однако для выявления легких степеней нарушения углеводного обмена необходимо исследование сахарной кривой с двойной нагрузкой глюкозой (см. Углеводы, методы определения). При нарушениях внешнесекреторной функции поджелудочной железы обычно выявляется более или менее выраженная гипопротеинемия; в более тяжелых случаях — нарушение электролитного обмена, в частности гипонатриемия (см.). Определение в дуоденальном содержимом, а также в крови и моче содержания ферментов поджелудочной железы позволяет дать оценку функц, состояния органа. В дуоденальном содержимом, полученном с помощью двухканального зонда (см. Дуоденальное зондирование), до и после стимуляции поджелудочной железы секретином и панкреозимином определяют общее количество сока, его бикарбонатную щелочность, содержание трипсина, липазы и амилазы; в крови — содержание амилазы, липазы, антитрипсина; в моче — амилазы. Одновременное проведение исследования содержания панкреатических ферментов в дуоденальном соке, крови, а также амилазурии позволяет значительно точнее отразить состояние внешнесекреторной функции поджелудочной железы у больных хрон. П., чем раздельное проведение этих исследований в разные дни.
Гиперамилазурия, достигающая при хрон. П. иногда цифр 2048 — 4096 ед. (по Вольгемуту), выявляется чаще, чем гиперамилаземия, однако увеличение амилазы мочи (до 256—512 ед.) иногда наблюдается и при других заболеваниях органов брюшной полости.
Содержание ферментов в крови и моче повышается в период обострения П., а также при препятствиях к оттоку панкреатического сока (воспалительный отек головки железы и сдавление протоков, рубцовый стеноз большого сосочка двенадцатиперстной кишки и др.). В дуоденальном содержимом концентрация ферментов и общий объем сока в начальном периоде болезни могут быть несколько увеличенными, однако при выраженном атро-фически-склеротическом процессе в железе эти показатели снижаются.
Копрологическое исследование (см. Кал) выявляет повышенное содержание в кале непереваренной пищи (стеаторея, креаторея, ами-лорея, китаринорея). По мнению Осте да (W. J. Austad, 1979), стойкая стеаторея при хрон. П. появляется тогда, когда внешняя секреция поджелудочной железы снижается не менее чем на 90% .
Источник статьи: http://xn--90aw5c.xn--c1avg/index.php/%D0%9F%D0%90%D0%9D%D0%9A%D0%A0%D0%95%D0%90%D0%A2%D0%98%D0%A2
Панкреатит
Панкреатит — это острая или хроническая воспалительная деструкция поджелудочной железы. Проявляется опоясывающей болью, болевыми ощущениями или дискомфортом слева в подреберье, связанными с пищевыми погрешностями, диспепсией, полифекалией, нарастающим ухудшением общего состояния. Диагностируется с помощью общего и биохимического анализа крови, УЗИ, МРТ, КТ поджелудочной железы, ИФА кала, ЭРПХГ, лапароскопии. Для лечения проводят обезболивающую, инфузионную, антисекреторную, заместительную ферментную и антибиотикотерапию. По показаниям выполняют некрэктомию поджелудочной железы, оментобурсостомию, удаление кист и псевдокист.
МКБ-10
Общие сведения
Термин «панкреатит» объединяет группу острых и хронических заболеваний с воспалительным поражением поджелудочной железы (ПЖ). За последние 30 лет распространенность патологии увеличилась более чем в 2 раза, отмечается стойкая тенденция к ее омоложению, в том числе более частое развитие панкреатита у детей. Распространенность острой формы болезни составляет от 0,0175 до 0,0734%, хронической — от 0,4 до 5%. Острые панкреатиты в 3,5 раза чаще диагностируются у женщин, хронические — вдвое чаще у мужчин. В группу риска входят пациенты, злоупотребляющие алкогольными напитками и страдающие билиарной патологией. Актуальность своевременной диагностики заболевания обусловлена тяжестью его осложнений, особенно при остром течении.
Причины панкреатита
Воспалительное поражение поджелудочной железы может иметь различное этиологическое происхождение. Специалисты в сфере клинической гастроэнтерологии выделяют несколько групп провоцирующих факторов, под влиянием которых развивается острое или хроническое воспаление органа. Возможными причинами панкреатита считаются:
- Алкогольные эксцессы. Более чем у половины пациентов заболевание становится следствием употребления больших количеств спиртного. В структуре деструктивных форм болезни алкогольные панкреатиты составляют до 70%. Риск воспалительной деструкции панкреатической паренхимы возрастает при употреблении суррогатов.
- Панкреатобилиарная патология. У 20% больных панкреатит развивается на фоне желчнокаменной болезни в результате механической обструкции панкреатического протока конкрементами. Причинами заболевания также служат травмы живота, рак поджелудочной железы, стеноз сфинктера Одди и кисты желчного протока.
- Ятрогении. В 4-5% случаев провоцирующим фактором становится нарушение техники ретроградной холангиопанкреатографии и абдоминальных операций. Токсическое воспалительное поражение панкреатической паренхимы возможно при приеме ингибиторов АПФ, петлевых диуретиков, цитостатиков и препаратов, содержащих серу (медикаментозный панкреатит).
Группа риска включает больных сахарным диабетом, гиперпаратиреозом и другими формами гиперкальциемии, вирусными гепатитами В и С, эпидемическим паротитом, глистными инвазиями. В отдельных случаях встречается панкреатит при беременности, трансплантации почек, ишемическом повреждении панкреатических тканей при шоке, эмболии артерий. При развитии патологического состояния в ответ на действие конкретного фактора (заболевания ЖКТ, травмы и др.) панкреатит называют реактивным. В 20-30% случаев причины остаются неустановленными (идиопатическое заболевание), не исключена роль отягощенной наследственности.
Патогенез
Механизм развития панкреатита основан на аутолизе тканей поджелудочной железы ее собственными протеолитическими и липолитическими ферментами. Пусковым моментом заболевания является гиперсекреция фосфолипазы А-2, липазы, эластазы, химотрипсиногена, трипсиногена, зачастую сочетающаяся с внутрипротоковой гипертензией из-за функционального спазма сфинктера Одди или механической обструкции большого дуоденального сосочка. Под действием энзимов начинается деструкция железы, нарастают нарушения микроциркуляции, отек.
Попадание ферментов в системный кровоток приводит к повреждению мозга, легких, почек, других тканей и органов. При хроническом течении панкреатита преобладает диффузная дегенерация тканей, атрофируются панкреоциты. Железистые элементы постепенно замещаются соединительной тканью, что сопровождается снижением экзокринной функции ПЖ и ухудшением процессов переваривания в кишечнике. Одновременно в системе протоков органа образуются кисты и конкременты. При вовлечении в процесс островков Лангерганса падает выработка инсулина.
Классификация
Основной критерий систематизации форм панкреатита — динамика патологического процесса. Заболевание может быть ограниченным или распространенным острым с быстрым нарастанием симптоматики (интерстициальный панкреатит, стерильный и инфицированный панкреонекроз) или хроническим с преимущественно дегенеративными изменениями. По характеру поражения острое воспаление бывает геморрагическим, гнойным, жировым, смешанным. Основными критериями, положенными в основу отечественной клинико-морфологической классификации хронического панкреатита, являются:
- Морфологические признаки. Учитываются гистологические изменения в органе. Процесс может быть интерстициально-отечным, паренхиматозным, индуративным (фиброзно-склеротическим), псевдотуморозным (гиперпластическим), кистозным.
- Ведущая симптоматика. Различают болевую, гипосекреторную, астено-невротическую (ипохондрическую) формы панкреатита. При наличии нескольких симптомов диагностируют сочетанный вариант, при их малой выраженности — латентный.
- Особенности клинического течения. Хронический панкреатит бывает редко и часто рецидивирующим. При постоянном наличии симптоматики говорят о персистирующем течении заболевания.
- Этиология. Наиболее распространенными вариантами панкреатита являются билиарнозависимый и алкогольный. Также специалисты выделяют дисметаболическую, инфекционную, лекарственную и идиопатическую форму патологии.
- Наличие осложнений. Возможно неосложненное и осложненное течение. С учетом ведущего осложнения различают панкреатит с нарушением оттока желчи, портальной гипертензией, инфекционным воспалением, эндокринными нарушениями, патологией других органов и систем.
Симптомы панкреатита
Проявления патологии зависят от варианта течения и наличия сопутствующих заболеваний ЖКТ. При билиарном панкреатите преобладает болевой синдром в верхних отделах живота без четкой локализации, боль может иррадиировать в лопатку, плечо и околосердечную область. Болевые приступы развиваются после злоупотребления жирной или жареной пищей, приема газированных напитков, которые вызывают спазм сфинктера Одди. При сопутствующей ЖКБ в период обострения наблюдается желтуха.
Патогномоничным признаком острого панкреатита является триада Мондора — вздутие живота, боль и рвота. Болевые ощущения возникают внезапно, они очень интенсивны, иногда приводят к потере сознания. Боль опоясывающая, рвота многократная, не приносит облегчения. Для острого воспаления типично быстрое ухудшения общего состояния больного: выявляется тахикардия и резкое снижение АД, усиленная потливость, бледность кожных покровов.
При хронической патологии болевой синдром менее интенсивен, обычно определяется после погрешностей в диете. Со временем пациенты отмечают, что боли появляются реже и заменяются дискомфортом в левом подреберье. Хронический панкреатит характеризуется нарушениями стула: обнаруживается полифекалия (выделение большого количества кала), испражнения приобретают сероватый цвет и резкий зловонный запах. Язык сухой, обложен желтоватым налетом. На передней брюшной стенке в проекции ПЖ формируется участок атрофии подкожной клетчатки.
Осложнения
Без лечения образуются инфильтраты, которые переходят в гнойно-некротические флегмоны забрюшинного пространства. Возможен перитонит. При тяжелом течении возникает полиорганная недостаточность, при поражении трех и более систем летальность составляет около 85%. При хроническом процессе в поджелудочной железе выявляется фиброз и кальциноз, наблюдается внешнесекреторная недостаточность. Вследствие поражения островков Лангерганса возникает вторичный сахарный диабет. Отмечается формирование и нагноение истинных или ложных кист, кровотечения из патологически измененных вен вследствие региональной портальной гипертензии.
Диагностика панкреатитов
Постановка диагноза панкреатита может быть затруднена, поскольку клиническая картина часто имитирует патологию других отделов ЖКТ. Заподозрить заболевание можно при выявлении характерных физикальных симптомов. Наиболее информативными инструментальными и лабораторными исследованиями являются:
- Исследование панкреатических ферментов в крови. Повышение уровня альфа-амилазы в 3-4 раза (при норме до 50 Ед/л) в первые сутки указывает на острый процесс или обострение хронического воспаления. С 4 суток проводят измерение уровня липазы — диагностически значимо двукратное увеличение показателя.
- ИФА каловых масс. Анализ кала на панкреатическую эластазу-1 необходим для оценки недостаточности внешнесекреторной функции органа. Значение в диапазоне 50-100 мкг/г указывает на среднюю степень нарушения экзокринной деятельности, при показателе ниже 50 мкг/г устанавливают тяжелую степень.
- Сонография поджелудочной железы. Для острого панкреатита характерно увеличение и отечность органа, нечеткость контуров и неоднородность структуры. При хроническом заболевании в ходе УЗИ поджелудочной железы определяется ее уменьшение, деформация контуров, кистозные образования и кальцификаты.
- Томография. МРТ поджелудочной железы считается «золотым стандартом» диагностики болезней ПЖ. Метод позволяет четко визуализировать паренхиму, оценить структуру кист и некротических участков. КТ с внутривенным контрастированием проводится для изучения секвестров и зон некроза.
- ЭРХПГ. Ретроградная холангиопанкреатография имеет высокую диагностическую ценность при подозрении на билиарный панкреатит, дает возможность оценить состояние сфинктера Одди, обнаружить белковые «пробки», конкременты и стриктуры протоков.
При низкой информативности других методов выполняют лапароскопию. В общем анализе крови определяют повышение СОЭ и нейтрофильный лейкоцитоз, степени изменения показателей коррелируют с тяжестью состояния пациента. В биохимическом анализе крови выявляют диспротеинемию, гипоальбуминемию, в случае панкреонекроза – высокие уровни АЛТ и АСТ. Дополнительно определяют концентрацию С-реактивного белка — значение более 120 мг/л свидетельствует об инфекционной природе заболевания.
Дифференциальный диагноз при остром процессе проводят с другой хирургической патологией, сопровождающейся симптомами «острого живота». Основные критерии: повышение амилазы, наличие УЗИ- и КТ-признаков поражения ПЖ. Хронический вариант панкреатита дифференцируют с большой группой воспалительных процессов ЖКТ с учетом анамнеза, жалоб и результатов дополнительных исследований. Пациента консультирует специалист-гастроэнтеролог, хирург, инфекционист.
Лечение панкреатита
Выбор терапевтической тактики определяется формой заболевания. Пациентам с острым процессом рекомендована госпитализация, функциональный покой органа (голодание, энтеральное зондовое или парентеральное питание). При хроническом воспалении необходима коррекция рациона с исключением спиртного, ограничением жиров и углеводов. Ведущей является консервативная медикаментозная терапия, которая с учетом клиники панкреатита может включать:
- Обезболивающие препараты. Обычно используют ненаркотические анальгетики, которые при наличии спастических дискинезий дополняют миотропными спазмолитиками. При интенсивном болевом синдроме показана эпидуральная блокада, введение наркотиков.
- Инфузионная терапия. Особую роль внутривенное вливание больших объемов электролитов играет при предупреждении панкреонекроза у больных с острым панкреатитом. Пациентам с хроническим воспалением инфузии обычно осуществляют при обострении болезни.
- Блокаторы желудочной секреции. Применение блокаторов протонной помпы и ингибиторов Н2-рецепторов позволяет снизить секрецию соляной кислоты и связанную с ней продукцию секретина. В результате уменьшается производство панкреатического сока.
- Ферменты поджелудочной железы. Заместительная терапия рекомендована при хроническом варианте панкреатита. Назначение комплекса панкреатических энзимов направлено на улучшение процессов переваривания и всасывания питательных веществ в кишечнике.
- Антибиотики. Используются преимущественно при остром воспалительном процессе для купирования и профилактики инфекционных осложнений. Наиболее эффективны фторхинолоны в комбинации с нитроимидазолами, карбапенемы, цефалоспорины 3-4 поколения.
При тяжелой форме применяют октапептиды, селективно угнетающие панкреатическую секрецию, проводят интенсивную терапию для поддержания АД, стабилизации метаболических нарушений. Пациентам с установленной этиологией панкреатита показано лечение основного заболевания. При остром панкреонекрозе может выполняться некрэктомия поджелудочной железы, оментобурсостомия. При стойких болях, связанных с наличием кистозных образований, производится удаление ложных кист поджелудочной железы или марсупиализация истинных кист.
Прогноз и профилактика
В случае острой патологии прогноз для пациентов сомнительный, исход заболевания обычно оценивают по шкале Рэнсона — наличие менее 3-х признаков свидетельствует об относительно благоприятном течении. Прогноз при хроническом панкреатите зависит от давности болезни и степени структурных поражений железы. Для профилактики воспаления необходимо ограничить потребление жирной пищи и газированных напитков, отказаться от вредных привычек (алкоголь, курение), проводить своевременное лечение заболеваний билиарной системы.
Источник статьи: http://www.krasotaimedicina.ru/diseases/zabolevanija_gastroenterologia/pancreas-inflammation